将0.1 mol的镁、铝混合物溶于100mL 2mol·L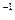 的H2SO4溶液中,然后再滴加1mol·L
的H2SO4溶液中,然后再滴加1mol·L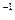 的NaOH溶液。请回答:(不需要写出计算过程)
的NaOH溶液。请回答:(不需要写出计算过程)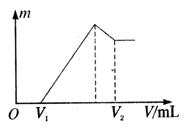
(1)若在滴加NaOH溶液的过程中沉淀质量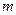 随加入NaOH溶液的体积V变化如图所示。当
随加入NaOH溶液的体积V变化如图所示。当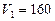 mL时,则金属粉末中
mL时,则金属粉末中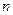 (Mg)= mol,
(Mg)= mol,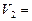 mL。
mL。
(2)①要配制100 mL 2mol·L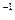 的H2SO4溶液,需要的仪器除量筒、烧杯外,还有 。
的H2SO4溶液,需要的仪器除量筒、烧杯外,还有 。
②下列操作会使所配的溶液浓度偏小的是( )(填代号)
| A.用量筒量取一定体积的98%的浓H2SO4,稀释后未经冷却即转入容量瓶内 |
| B.稀释硫酸所用的小烧杯未洗涤 |
| C.定容时俯视液面 |
| D.用蒸馏水洗涤后的容量瓶未干燥 |
E.定容摇匀后,倒入干燥的试剂瓶中储存时,有少量溶液浅出瓶外
0.5mol H2SO4的质量是g,含个氧原子,能和molNaOH完全反应,该硫酸所含氢元素的质量与mol H3PO4或标准状况下L HCl中所含氢元素的质量相同。
成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成份的存在,请你参与并协助他们完成相关实验。
(1)用小试管取少量的苹果汁,加入 ,溶液变蓝,则苹果中含有淀粉。
(2)用小试管取少量的苹果汁,加入新制Cu(OH)2悬浊液,并加热,产生砖红色的沉淀,则苹果中含有
(写分子式)。
(3)葡萄糖在一定条件下可以得到化学式为C2H6O的化合物A。
A + CH3COOH→有香味的产物
① 含A的体积分数为75%的水溶液可以用做 。
②写出化合物A与CH3COOH反应的化学方程式为 ,该反应的类型为 。
(4)苹果中含有苹果酸,测得其相对分子质量为134。取0.02mol苹果酸,使其完全燃烧,将燃烧后的产物先后通过足量的无水CaCl2和碱石灰,两者分别增重1.08g和 3.52g。则分子中C、H原子的个数比 。苹果酸的分子式是 。
铁及铁的化合物应用广泛,如FeCl3可用做催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式是______________________。
(2)若将1中的反应设计成原电池,请画出原电池的装置图__________________(标出正、负极材料及电解质溶液),并写出电极反应式。
正极反应________________,负极反应__________________。
(3)某科研人员发现劣质不锈钢在某些盐溶液中腐蚀现象明显。请从提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu中选择两种水可任选,设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式①_____________________________
②_____________________________。
劣质不锈钢腐蚀的实验现象_____________________________。
(4)Li—SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2=== 4LiCl+S+SO2。该电池正极发生的电极反应为____________________________。
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚(CH3OCH3)。
请回答下列问题:
(1)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:
(2)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)  CH3OH(g)△H=-90.8 kJ·mol-1
CH3OH(g)△H=-90.8 kJ·mol-1
② 2CH3OH(g)  CH3OCH3(g) + H2O(g) △H=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g) △H=-23.5 kJ·mol-1
③ CO(g) + H2O(g)  CO2(g) + H2(g) △H=-41.3 kJ·mol-1
CO2(g) + H2(g) △H=-41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2 (g)的 △H=
CH3OCH3(g) + CO2 (g)的 △H=
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是:
(填字母代号)。
a.压缩体积 b.加入催化剂
c.减少CO2的浓度 d.增加CO的浓度
e.分离出二甲醚(CH3OCH3)
(3)已知反应②:2CH3OH(g)  CH3OCH3(g) + H2O(g) △H=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g) △H=-23.5 kJ·mol-1
某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度(mol·L-1) |
0.40 |
0.6 |
0.6 |
① 比较此时正、逆反应速率的大小比较:v正v逆(填“>”、“<”或“=”)。
②该反应的平衡常数的表达式为K=温度升高,该反应的平衡常数K
(填“增大”、“减小”或“不变”)
某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
1根据下表中数据,在下图中画出X、Y、Z的物质的量n随时间t变化的曲线:
| t/min |
X/mol |
Y/mol |
Z/mol |
| 0 |
1.00 |
1.00 |
0.00 |
| 1 |
0.90 |
0.80 |
0.20 |
| 3 |
0.75 |
0.50 |
0.50 |
| 5 |
0.65 |
0.30 |
0.70 |
| 9 |
0.55 |
0.10 |
0.90 |
| 10 |
0.55 |
0.10 |
0.90 |
| 14 |
0.55 |
0.10 |
0.90 |

2体系中发生反应的化学方程式是_____________;
3列式计算该反应在0~3 min时间内产物Z的平均反应速率:______________________;
4该反应达到平衡时反应物X的转化率α等于________;
5如果该反应是放热反应。在该反应达到上述平衡状态时改变实验条件温度、压强、催化剂得到Z的物质的量(mol)随时间t(min)变化的曲线1、2、3如上右图所示则曲线1、2、3所对应的实验条件改变分别是:1______________,2______________,3______________。