已知V、W、X、Y、Z五种短周期元素的原子序数依次增大,在周期表中W与V、X相邻,Y与Z相邻,X与Y同主族,W的气态氢化物可与Z的气态氢化物反应生成盐。请回答下列问题:
(1)X元素在周期表中位置是 ;
(2)Y的离子结构示意图是 ;
(3)V的单质与Y的最高价氧化物的水化物反应的化学方程式为:
;
(4)V元素可形成化合物Fe(AO)5,该物质常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(AO)5晶体属于 晶体(填晶体类型);
(5)Y2Z2分子中,Y与Z均满足8e-稳定结构,则Y2Z2的电子式为 ;
(6)Z的单质与澄清石灰水反应的离子方程式为:
。
工业制硫酸生产流程如下图:
(1)实验室常用过量的氢氧化钠溶液吸收SO2尾气,该反应的离子方程式为。
(2)已知SO2和O2生成SO 3的反应过程放热。在催化反应室中,下列措施有利于提高SO2平衡转化率的有。(填写编号)
A.减少压强 B.升高温度 C.不断补充空气 D.及时分离出SO3
(3)在工业制硫酸生产中,为提高催化剂效率采取的措施有(答出2点)。
(4)在450℃、常压和钒催化条件下,在容积为2L的恒容容器中加入2molSO2和1molO2 。
①下列选项中不能作为判断该反应是否达平衡状态的标志的是。(填写编号)
A.混合气密度不变化
B.SO2百分含量保持不变
C.容器中气体的压强不变
D.SO3的生成速率与SO2的消耗速率相等
E.气体总物质的量不变
②达平衡后,测得平衡常数为K,若此时O2的转化率为x,则K和x的关系满足K=。
(5)SO2和O2的反应在恒容密闭容器中发生,图1、2表示在时刻t1达到平衡、在时刻t2因改变某个条件而发生变化的情况,根据图1、图2相关信息,判断t2发生改变的条件是。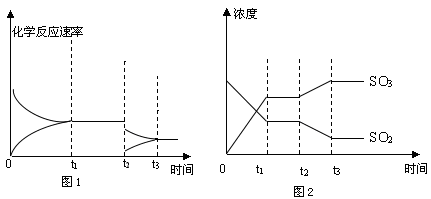
某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1 mol·L-1 FeCl2溶液,实验记录如下(a、b、c代表电压值):
| 序号 |
电压/V |
阳极现象 |
检验阳极产物 |
| Ⅰ |
x≥a |
电极附近出现黄色,有气泡产生 |
有Fe3+、有Cl2 |
| Ⅱ |
a>x≥b |
电极附近出现黄色,无气泡产生 |
有Fe3+、无Cl2 |
| Ⅲ |
b>x>0 |
无明显变化 |
无Fe3+、无Cl2 |
(1)用KSCN溶液检验出溶液中含Fe3+,看到的现象是_____。
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出Cl2氧化Fe2+的离子方程式:______________________________________。
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电。原因是Fe2+具有____性。
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证。控制变量,做对照实验继续探究:电解pH=1的NaCl溶液,记录如下:
| 序号 |
电压/V |
阳极现象 |
检验阳极产物 |
| Ⅳ |
a>x≥c |
无明显变化 |
有Cl2 |
| Ⅴ |
c>x≥b |
无明显变化 |
无Cl2 |
①NaCl溶液的浓度应是______mol·L-1。
②Ⅳ中检验Cl2的实验方法:________________________________。
③与Ⅱ对比,得出的结论:通过控制电压,证实了产生Fe3+的两种原因都成立;通过控制电压,验证了放电顺序是:Fe2+___________Cl-(填“>”或“<”)
(14分)对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
①碱洗的目的是除去铝材表面的自然氧化膜。碱洗时常有气泡冒出,该气体的名称为。
②为将碱洗槽液中的铝元素以沉淀形式回收,最好向槽液中加入下列试剂中的。
A.NH3 B.CO2 C.NaOHD.HNO3
③以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是。
(3)下列关于金属腐蚀的事实中,与电化学腐蚀有关的是
A.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀
B.为保护海轮的船壳,常在船壳上镶入锌块
C.在空气中,金属银的表面生成一层黑色物质
D.镀银的铁制品,镀层部分受损后,露出的铁表面易被腐蚀
(4)利用下图装置,可以模拟铁的电化学防护。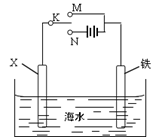
①若X为碳棒,为减缓铁的腐蚀,开关K应置于处。
②若X为锌,开关K应置于处。
思考下列问题,按要求填空:
(1)某温度下纯水中c(H+) = 2×10-7 mol/L
①此时溶液中的C(OH-) = _____。
②若温度不变,向水中滴入稀盐酸使c (H+) = 5×10-6 mol/L,则此时溶液中的C(OH-) =_____。
(2)已知下列热化学方程式:Zn(s)+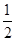 O2(g)="==ZnO(s)" △H1="-351.1" kJ·mol-1;
O2(g)="==ZnO(s)" △H1="-351.1" kJ·mol-1;
Hg(l)+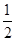 O2(g)="==HgO(s)" △H2="-90.7" kJ·mol-1
O2(g)="==HgO(s)" △H2="-90.7" kJ·mol-1
由此可知反应Zn(s)+HgO(s)===ZnO(s)+Hg(l)的焓变为_____。
(3)在稀氨水中存在下述电离平衡NH3+H2O  NH3 ·H2O
NH3 ·H2O  NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?_____(填“增大”、“减小”或“不变”);平衡移动方向如何?_____(填“正向”、“逆向”或“不移动”)。
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?_____(填“增大”、“减小”或“不变”);平衡移动方向如何?_____(填“正向”、“逆向”或“不移动”)。
| 加入的物质 |
少量(NH4)2SO4固体 |
少量HNO3溶液 |
少量KOH溶液 |
| c(OH-)的变化 |
减小 |
||
| 平衡移动方向 |
逆向 |
逆向 |
(4)如图所示,装置B中两电极均为石墨电极,试回答下列问题:
①判断装置的名称:A池为________。
②锌极为______极,电极反应式为____________;
③当C2极析出224 mL气体(标准状况下),锌的质量减少__g
已知拆开1 mol H—H键、1 mol I—I、1 mol H—I键分别需要吸收的能量为436kJ、151k J、299k J。则由氢气和碘反应生成2mol HI需要(填“放出”或“吸收”)11k J的热量。此反应中反应物的总能量(填“大于”或“小于”)生成物的总能量。物质具有的能量越(填”高”或”低”)越稳定。