用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.lmol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现 象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处 、
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
由分子式及核磁共振氢谱写出该有机物的结构简式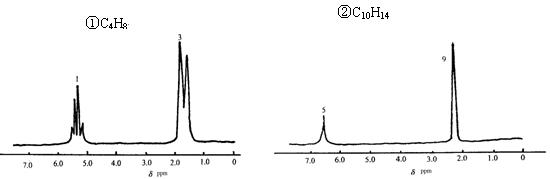
①结构简式:________________________②结构简式:________________________
镁及其化合物在生产生活中有重要的作用。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为。指出该物质在工农业生产中的一种用途:。
(2)写出预氨化时发生的主要反应的离子方程式:。
(3)沉淀镁时反应的温度不宜过高,原因是。
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③;④;⑤称量MgO。
18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a=;b =;c =。
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁。有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则。你同意该同学的想法吗?为什么?你的观点是。理由是。
下面是某纤维的合成路线(部分反应未注明条件):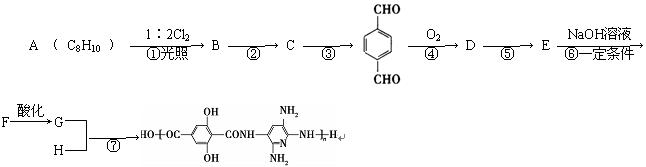
根据以上合成路线回答下列问题:
(1)A的名称是,苯环上的一氯取代物有
种。
(2)反应②的条件是,反应③的条件是。
(3)写出反应④和⑦的化学反应方程式
④、⑦。
(4)符合下列条件的D的同分异构体有种。
①能使FeCl3溶液显紫色②含氧官能团的种类相同
(14分)现有前20号的A、B、C、D、E五种元素,相关信息于下表:
| 元素 |
信息 |
| A |
元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B |
B原子得一个电子后2p轨道全满 |
| C |
C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大 |
| D |
D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于其中子数 |
| E |
E+和B- 具有相同的电子层结构 具有相同的电子层结构 |
(1)B的核外电子排布式为________,CB3的晶体类型为________ 。
(2)B、C、D三元素的电负性大小顺序为________>________>________(填元素符号)。
(3)C的氢化物的空间构型为________,其氢化物在同族元素所形成的氢化物中沸点最高的原因是______________________________________________________。
(4)E2D的水溶液呈(填“酸性”、“碱性”或“中性”),用离子方程式解释理由:_______________________。
(5)已知:12.8 g液态C2 A4与足量A2O2反应生成C2和气态A2O,放出256.65 kJ的热量。
A2O (l)=== A2O (g) ΔH=+44 kJ·mol-1。
2 A2O2 (l)===2A2O (l)+O2(g) ΔH=-196.4 kJ·mol-1。
则液态C2 A4与足量O2反应生成C2和液态A2O的热化学方程式为: ________________________________________________。
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。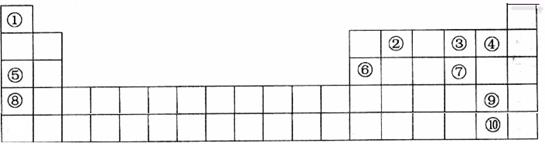
用化学符号回答下列问题:
(1)表中最活泼的金属与最活泼的非金属形成的物质是_______ ___;
(2)⑤、⑥、⑧的最高价水化物的碱性由强到弱的顺序是;
③、④、⑦氢化物稳定性由强到弱的顺序是;
(3)①与⑤按原子个数1:1所成的化合物的电子式为________________ _;该化合物与水反应的离子方程式为________________ _。
(4)⑥号元素最高氧化物水化物与⑤号元素最高价氧化物水化物反应的离子方程式为__________;
(5)请设计一个实验方案,比较⑨、⑩的单质氧化性的强弱:。