下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。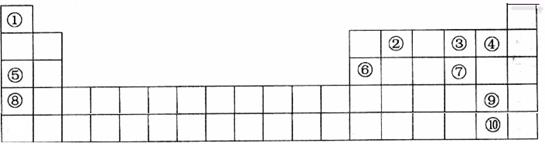
用化学符号回答下列问题:
(1)表中最活泼的金属与最活泼的非金属形成的物质是_______ ___;
(2)⑤、⑥、⑧的最高价水化物的碱性由强到弱的顺序是 ;
③、④、⑦氢化物稳定性由强到弱的顺序是 ;
(3)①与⑤按原子个数1:1所成的化合物的电子式为________________ _ ;该化合物与水反应的离子方程式为________________ _ 。
(4)⑥号元素最高氧化物水化物与⑤号元素最高价氧化物水化物反应的离子方程式为__________ ;
(5)请设计一个实验方案,比较⑨、⑩的单质氧化性的强弱: 。
维生素A是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致干眼病、夜盲症、皮肤干燥等多种病症。右图是维生素A的结构。
请回答:
(1)维生素A的分子式为
(2)下列物质在一定条件下能与维生素A反应的是(填标号)
| A.溴水 | B.酸性高锰酸钾溶液 | C.乙酸 | D.新制CuO E.NaOH溶液 |
(3)如果有机物分子中所含氢原子个数比其同碳原子数少的“烷”少,称为“缺氢指数”或“不饱和度”,如 和环丙烷的不饱和度为1,
和环丙烷的不饱和度为1,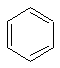 和
和 的不饱和度为4。由此推断,维生素A的不饱和度为
的不饱和度为4。由此推断,维生素A的不饱和度为
按要求填空
(1)乙烯的电子式
(2)环己烷的键线式
(3)由溴乙烷制取乙二醇,依次发生反应的类型是、、
完成下列反应方程式
(1)乙醇与金属钠反应
(2)乙烯和溴的四氯化碳溶液反应
(3)苯乙烯一定条件下生成聚苯乙烯
(4)甲苯与浓硝酸、浓硫酸的混合酸在100℃下的反应
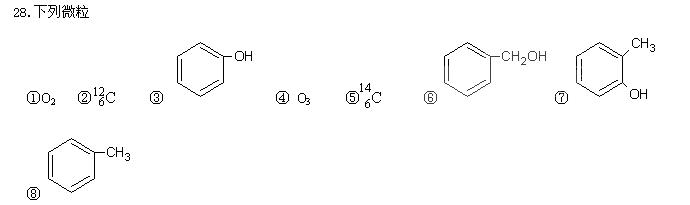 (1)属于同位素的是(填编号,下同)
(1)属于同位素的是(填编号,下同)
(2)属于同素异形体的是
(3)属于同分异构体的是
(4)属于同系物的是
某固体混合物可能由Al、(NH4)2SO4、MgCl2 、AlCl3、CuCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体
、AlCl3、CuCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体 体积数据已换算成标准状况下的体积):
体积数据已换算成标准状况下的体积):
回答下列问题:
⑴混合物中是否存在CuCl2(填“是”或“否”);
⑵混合物中是否存在(NH4)2SO4(填“是”或“否”),你的判断依据是。
⑶写出反应③中的离子方程式
。
(4)请根据计 算结果判断混合物中是否含有AlCl3(说出你的计算依据,不要求写计算过程)。
算结果判断混合物中是否含有AlCl3(说出你的计算依据,不要求写计算过程)。
___________________________________________________________________________。