雌二醇和睾丸素均属类固醇类化合物,该类化合物的结构特征是均含有相同的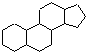 “三室一厅”的核心构架。这两种化合物的结构简式如下:
“三室一厅”的核心构架。这两种化合物的结构简式如下:
下列叙述中,不正确的是
| A.均能与卤化氢发生取代反应 |
| B.均能发生脱水的消除反应 |
| C.均可使溴水褪色 |
| D.两种物质的分子组成相差一个CH2,但不属于同系物 |
下列叙述不能作为元素周期表中元素排列顺序依据的是
| A.原子的核电荷数 | B.原子的中子数 |
| C.原子的质子数 | D.原子的核外电子数 |
下列粒子中,只有还原性的是
| A.Br- | B.H+ | C.Mg2+ | D.H2O |
下列物质中,不含有硅酸盐的是
| A.水玻璃 | B.硅芯片 | C.黏土 | D.普通水泥 |
下列反应属于自然氮的固定作用的是
| A.N2和H2一定条件下反应制取NH3 | B.硝酸工厂用NH3氧化制取NO |
| C.雷雨时空气中的N2转化为NO | D.由NH3制碳酸氢铵和硫酸氨 |
关于室温下下列溶液的说法不正确的是
| 编号 |
① |
② |
③ |
④ |
| 溶液 |
氨水 |
氢氧化钠溶液 |
盐酸 |
醋酸溶液 |
| pH |
11 |
11 |
3 |
3 |
A.水的电离程度:①=②=③=④
B.分别加水稀释10倍,溶液的pH:①>②>③>④
C.①、③两溶液等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.V1L②溶液与V2 L③溶液混合,若混合溶液pH=4,则V1:V2=9:11(忽略溶液体积变化)