有X、Y、Z、W、M、N六种短周期元素,其中X、Y、Z、W同周期,Z与M、N与Y分别同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。
(1) 元素X与 M形成X2M2型化合物中阴阳离子个数比为:____________
(2) YM2晶体属于_____________晶体(填晶体类型);30g YM2晶体中含_________条共价键(阿伏加德罗常数用NA表示)
(3) 在工业上常用电解饱和XW的溶液来制碱。若用阴极室产生的气体为碱性燃料电池的燃料,则燃料电池中该气体所在电极为_______极,电极反应式为:_________________。
(4) 已知单质A为常见黑色固体粉末,B是元素Z的最高价含氧酸,其存在如图所示的转换关系: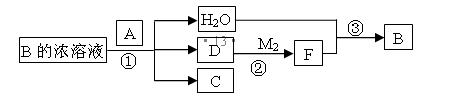
(I) 若向C中滴加KSCN溶液立即呈血红色。则:常温下A在B的浓溶液中难以溶解的原因是 ;因此反应①的的条件是 。在工业上反应③是在___________(填设备)中进行的;在实验室用________(填药品名)检验D的存在;含D的尾气直接排放到大气中造成环境污染的后果是 ;
(II) 按要求写方程式:
写出反应②的化学方程式 ,
写出C与小苏打溶液反应的离子方程式 ,
(III) 若A是元素N的单质写出反应①的化学方程式:___________________。
有A、B、C、D、E和F六瓶无色溶液,他们是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1)能确定溶液是(写出溶液标号与相应溶质的化学式):
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的转换关系如下图所示(部分产物略去)。
(1)若A为单质,组成A单质的元素是自然界中形成化合物种类最多的元素。
①B属于分子(填“极性”或“非极性”),B分子中所有原子是否都满足8电子结构,(填“是”或“否”)。
②向50 mL 4 mol/L的NaOH溶液中通入1.12 L B(标准状况),反应后溶液中的溶质为_______(填化学式),物质的量分别为_____________。
(2)若A为第三周期中的元素所形成的氯化物。
①写出A溶液→B的离子方程式。
②写出A和B在溶液中反应的离子方程式。
(3)若A为常见的金属,在E的冷、浓溶液中有钝化现象。已知:X为含有非极性键的离子化合物,且1 mol X含有38 mol电子,向D溶液中加入与D等物质的量的固体X,该反应的离子方程式为。
盐酸、硫酸和硝酸是中学阶段常见的三种强酸。请就三者与金属铜的反应情况,回答下列问题:
(1)
①在100mL 18molL-1的 浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是。
浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是。
A.40.32L B.30.24L C.20.16L D.6.72L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式。
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是 ,反应中所消耗的硝酸的物质的量可能为。
A.0.1mol B.0.15mol C.0.2mol D.0.25mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为。
甲.乙.丙.丁均具有如图所示的结构或结构单元。实线表示共价键,X.Y可同可不同。
已知:甲.乙晶体类型相同,单质甲能与乙发生置换反应,丙.丁.戊三种粒子均含有等量的总电子数,其中丙.戊是同一类晶体中的分子,戊在常温下呈液态,能产生两种10电子的离子,丁是阳离子且与丙符合“等电子原理”(具有相同电子数和原子数的分子或离子互称为等电子体)。
(1)写出液态戊产生两种等电子粒子的电离方程式:。
(2)写出甲与乙发生置换反应的反应方程式:。
(3)丙是目前重要的能源之一。
① 丙和戊在催化.加热条件下得到可燃性的两种气体,其反应的化学方程式是:。
② 现代高能电池中,常用丙作燃料电池的原料,在碱性介质(KOH溶液)的情况下,其负极反应的电极方程式为。
(4)含丁的硝酸盐溶液显酸性,原因是(用离子方程式表示):
Ⅰ.在一定温度下,把2 mol N2和6 mol H2通入一个体积不变的密闭容器中(如下图)发生反应:N2(g)+3 H2(g)2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7 mol 。据此回答下列问题: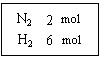
保持上述反应温度不变,使a.b.c分别代表初始加入的N2.H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
(1)若a =" 1" mol,c ="2" mol ,则b ="____" mol,在此情况下,
反应起始时将向方向进行(填 “正”或“逆”)
(2)若规定起始时反应向逆反应方向进行,则c的取值
范围是。
(3)在上述装置中,若需控制平衡后混和气体的物质的量为6.5 mol,则可采取的措施是
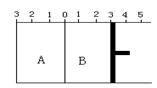
Ⅱ.如图所示,温度不变时,把某容器分割成A.B两部分,A容器体积固定不变,B有可移动的活塞,现在A中充入2 mol SO2和1 mol O2,在B中充入2 mol SO3和 1 mol N2,在相同条件下发生可逆反应:
2 SO2(g)+O2(g)  2 SO3(g)。
2 SO3(g)。
根据下列要求填写空白:
(1)固定活塞位置在3处不动,达到平衡时,
设A中压强为PA,B中压强为PB,则
PA与PB的关系是PAPB(填“<”.“=”.“>”)。
(2)若要使A与B中平衡状态相同,可移动活塞的位置应在处。
(3)若活塞右移到5处,达到平衡后,B中SO3为x mol,A中SO3为y mol , 则x和y 的关系是x y.(填“<”.“=”.“>”)。