下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的500mL稀H2SO4溶液的操作,请按要求填空:
(1)所需浓H2SO4的体积为 mL。
(2)如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配 溶液浓度将 (偏高、偏低、无影响)。
溶液浓度将 (偏高、偏低、无影响)。
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL蒸馏水的 里,并不断搅拌。
(4)将冷却至室温的上述溶液沿 注入 中,并用蒸馏水洗涤烧杯2~3次,洗涤液也要注入其中,并摇匀。
(5)加水至距刻度线下 cm时,改用 加水,使溶液的凹液面正好跟刻度相切。
甲醇是一种可再生能源,具有广泛的开发和应用前景.请回答下列与甲醇有关的问题.
(1)甲醇分子是____________分子(填“极性”或“非极性”)。
(2)工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)  CH3OH(g)△H=﹣86.6KJ/mol,在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2,反应达到平衡时,容器内的压强是开始时的3/5.
CH3OH(g)△H=﹣86.6KJ/mol,在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2,反应达到平衡时,容器内的压强是开始时的3/5.
①达到平衡时,CO的转化率为____________
②下列选项能判断该反应达到平衡状态的依据的有____________
| A.2v(H2)=v(CH3OH) | B.CO的消耗速率等于CH3OH的生成速率 |
| C.容器内的压强保持不变 | D.混合气体的密度保持不变 |
E.混合气体的颜色保持不变 F.混合气体的平均相对分子质量不随时间而变化
(3)已知在常温常压下:
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H=﹣akJ·mol﹣1
②2CO(g)+O2(g)=2CO2(g)△H=﹣bkl·mol﹣1
③H2O(g)=H2O(1)△H=﹣ckJ·mol﹣1
则CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=____________kJ·mol﹣1
(4)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为____________________.
②若以该电池为电源,用石墨做电极电解200mL含有如下离子的溶液.
| 离子 |
Cu2+ |
H+ |
Cl﹣ |
SO42﹣ |
| c/mol·L﹣1 |
0.5 |
2 |
2 |
0.5 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为____________.
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ 的热量。
(1)写出该反应的热化学方程式________________________。
(2)已知H2O(l)=H2O(g);△H=+44kJ·mol-1,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是_____________kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是___________________。
(4)已知N2(g)+2O2(g)="2" NO2(g);△H=+67.7 kJ·mol-1, N2H4(g)+O2(g)=N2(g)+2H2O (g);△H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式____________________。
Ⅰ、可逆反应:aA(g) + bB(g) cC(g) + dD(g);根据图回答:
cC(g) + dD(g);根据图回答:
①压强 P1 P2;(a +b) (c +d)(填“>”或“<”下同)。
②温度t1℃ t2℃;△H 0。
③保持体积和温度不变,通入He,平衡会_________________移动(填“正向”、“逆向”或“不”)。
Ⅱ、写出下列元素基态原子的电子排布式:
①29Cu____________________
②32Ge(简式)____________________
下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明。请根据此表,结合初中化学和生物学科的知识,回答下列问题。
| 配料表 |
精制海盐、碘酸钾 |
| 含碘量 |
20~40mg/kg |
| 卫生许可证号 |
××卫碘字(1999)第001号 |
| 分装日期 |
见封底 |
| 储藏方法 |
密封、避光、防潮 |
| 食用方法 |
烹调时,待食品熟后加入碘盐 |
(1)碘是合成下列哪种激素的主要原料之一()
A.胰岛素 B.甲状腺素 C.生长激素D.雄性激素
(2)长期生活在缺碘山区,又得不到食盐供应,易患()
A.甲状腺亢进B.贫血症C.地方性甲状腺肿大 D.糖尿病
(3)食盐中加碘,这碘指的是 (填元素、原子或单质)。
(4)碘酸钾的化学式为KIO3,其中碘元素的化合价为____________。
(5)根据含碘盐的食用方法可推测碘元素的化学性质,碘酸钾在受热时容易______ ____。
(6)已知可用盐酸酸化的碘化钾淀粉溶液,检查食盐中含碘酸钾(进行如下反应:IO3-+5I-+6H+==3I2+3H2O)。现有①纯净水、②白酒、③食醋、④淀粉KI试纸、⑤纯碱,试从中选择必须的物质检验食盐样品中是否加入碘,选择的物质_______________(填序号)。
有如下有机物:
①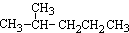 ②
②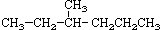 ③
③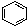
④CH3CH=CHCH3 ⑤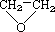 ⑥
⑥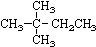 ⑦
⑦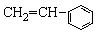
(1)互为同分异构体的是:__________,存在手性异构体的是:____________,存在顺反异构体的是__________,互为同系物的是(任写一对):__________;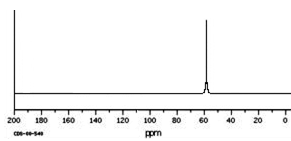
(2)氢核磁共振(1H-NMR)图谱如上图所示的有_______________________;
(3)上述物质中,不属于同分异构体,相同质量时,在氧气中完全燃烧消耗的氧气的质量完全相同的烃是:____________________;
(4)有机物④的系统命名法名称是_____________________;
(5)有机物⑤的键线式_____________,其分子中碳原子_______杂化。