研究NOx(氮的氧化物)SO2、CO等大气污染气体的测量及处理具有重要意义。
(1)下图是 反应过程中能量示意图。
反应过程中能量示意图。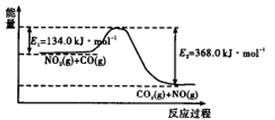
该反应的焓变
(2)一定条件下,通过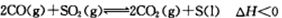 可以实现燃煤烟气中硫的回收。某研究小组向2L某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中通入CO和SO2,10分钟后测得容器CO2的物质的量为0.9mol。
可以实现燃煤烟气中硫的回收。某研究小组向2L某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中通入CO和SO2,10分钟后测得容器CO2的物质的量为0.9mol。
①求以v(CO2)表示的反应速率为 。
②该反应的平衡常数的表达式为:K= 。
③若想加快正反应速率的同时提高SO2的转化率,可以采用的方法是 。
(3)工业上常用Na2CO3溶液吸收法处理氮的氧化物(以NO和NO2的混合物为例)。
已知:NO不能与Na2CO3溶液反应。
若用足量的Na2CO3溶液完全吸收NO和NO2的混合物,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则混合气体中NO和NO2的体积比为 。
如图所示,若电解5 min 时铜电极质量增加2.16 g,试讨论:
时铜电极质量增加2.16 g,试讨论: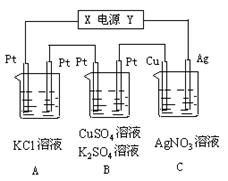
⑴电源电极X名称为_________。
⑵ pH变化:A_______,B______,C______。
⑶通过5 min时,B中共收集224 mL气体(标况),溶液体积为200mL,则通电前硫酸铜溶液的物质的量浓度为______________。
⑷若A中KCl溶液的体积也是2 00 mL,且电解过程中体积不变,电解后溶液中的氢氧根离子浓度是__________
00 mL,且电解过程中体积不变,电解后溶液中的氢氧根离子浓度是__________ 。
。
2A B + C在某一温度时,达到平衡。
B + C在某一温度时,达到平衡。
(1)若温度升高,平衡向正反应方向移动,则正反应是_________反应(填放热或吸热);
(2)若B为固体,降低压强平衡 向逆反应方向移动,则A呈___________态;
向逆反应方向移动,则A呈___________态;
(3)若A是气态时,加压时,平衡不移动,则B为_________态,C为__________态;
(4) 若A、B、C均为气体,加入催化剂,平衡___________移动(填 正向、逆向、不)
正向、逆向、不)
煤作为燃料有两种途径:
Ⅰ.C(s)+O2(g)===CO2(g) ΔH1<0
Ⅱ.C(s)+H2O(g)===CO(g)+H2(g) ΔH2>0
2CO(g)+O2(g)===2CO2(g) ΔH3<0
ΔH3<0
2H2(g)+O2(g)===2H2O(g) ΔH4<0
请回答:(1)途径Ⅰ放出的热量________途径Ⅱ放出的热量(填“>”、“<”或“=”)。
(2)ΔH1、ΔH2、ΔH3、ΔH4之间关系的数学表达式是________________。
如右图,a、b是石墨电极,Z是滴有酚酞的饱和氯化钠溶液,通电一段时间后,在a棒附近看到颜色变红明显,则电源y是极,实验过程中还能观察到的现象是
,a棒发生的电极反应式为,b棒电极反应式为。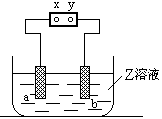
(10分)在密闭容器里,通入x mol H2(g)和y molI2(g),发生反应
H2(g)+I2(g) 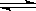 2HI(g)△H<0。改变下列条件,反应速率将如何改变?(填“增大”“减小”或“不变”)
2HI(g)△H<0。改变下列条件,反应速率将如何改变?(填“增大”“减小”或“不变”)
(1)升高温度;(2)扩大容器的体积;
(3)充入更多的H2;(4)容器容积不变,通入氖气;