煤作为燃料有两种途径:
Ⅰ.C(s)+O2(g)===CO2(g) ΔH1<0
Ⅱ.C(s)+H2O(g)===CO(g)+H2(g) ΔH2>0
2CO(g)+O2(g)===2CO2(g) ΔH3<0
ΔH3<0
2H2(g)+O2(g)===2H2O(g) ΔH4<0
请回答:(1)途径Ⅰ放出的热量________途径Ⅱ放出的热量(填“>”、“<”或“=”)。
(2)ΔH1、ΔH2、ΔH3、ΔH4之间关系的数学表达式是________________。
(共14分)SO2的含量是空气质量日报中一项重要检测指标,请结合所学知识回答下列问题。
(1)工业制硫酸过程中,SO2催化氧化的原理为:2SO2(g)+O2(g) 2SO3(g) 。T℃时,向某密闭容器中充入一定SO2(g)和O2(g),发生上述反应,测得SO2(g)的平衡转化率(a)与体系总压强(p)的关系如图所示。
2SO3(g) 。T℃时,向某密闭容器中充入一定SO2(g)和O2(g),发生上述反应,测得SO2(g)的平衡转化率(a)与体系总压强(p)的关系如图所示。
①a、b两点对应的平衡常数K(a) K(b)(填“>”、“<”或“=”,下同),SO2浓度c(a) c(b)。
②c点时,反应速率v(正) v(逆)。
(2)电化学法处理SO2。
硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如下图所示(电极均为惰性材料):
①M极发生的电极反应式为 。
②若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为 L(已知:1个e-所带电量为1.6×10-19C)。
(3)溶液法处理SO2。已知常温下H2SO3和H2CO3的电离常数如下表所示:
常温下,将SO2缓慢通入100mL 0.2mol•L-1的Na2CO3溶液中,当通入448mLSO2时(已折算为标准状况下的体积,下同),发生的离子方程式为 ;当通入896mLSO2时,所得溶液呈弱酸性,溶液中各离子浓度由大到小的顺序为 。
(共14分)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
回答下列问题:
(1)步骤①中得到的氧化产物是_________,溶解温度应控制在60~ 70℃,原因是________ 。
(2)写出步骤③中主要反应的离子方程式___________。若向亚硫酸氢铵溶液中加入过量氢氧化钠溶液,反应的离子方程式为 。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是________ _。
(5)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________。
(共12分)氯元素是生产生活中常见的非金属元素。
(1)将Cl2通入NaOH溶液中得到以NaClO为有效成分的漂白液,写出该反应的离子方程式 ;不直接用Cl2作漂白剂的原因是 (写出两条)。
(2)使用Cl2为自来水消毒时,会与水中的有机物生成对人体有害的有机氯化物。下列物质中可以替代Cl2为自来水杀菌消毒的是 (填字母序号)。
a.臭氧b.NH3 c.明矾 d.ClO2
(3)生物质混煤燃烧是当今能源燃烧利用的最佳方式之一,但生物质中氯含量较多,燃烧过程中会形成金属氯化物(如NaCl)和Cl2等物质,对金属炉壁造成腐蚀。
①NaCl和Cl2中化学键的类型分别是 和 。
②燃煤过程中生成的SO2会与NaCl等物质发生反应,生成硫酸盐和Cl2。若生成Cl2 22.4 L(标况)时转移电子数为4×6.02×1023,该反应的化学方程式是 。
③已知:2H2O2(l)=2H2O(l)+O2(g)ΔH1 = -196.46 kJ·mol-1
H2(g)+1/2O2(g)= H2O(l)ΔH2 = -285.84 kJ·mol-1
Cl2(g)+H2(g)=2HCl(g)ΔH3 = -184.60 kJ·mol-1
在催化剂作用下,用H2O2(l)可除去上述燃烧过程中产生的Cl2。依据上述已知反应,写出该反应的热化学方程式: 。
B:【化学—选修5有机化学基础】芳香族化合物A常用来合成药物B及医药中间体G,其流程如图: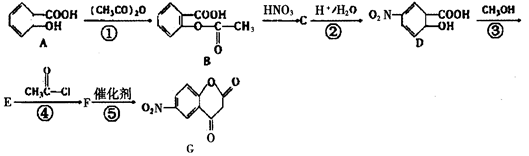
已知: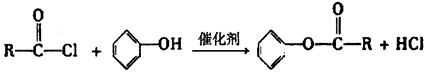
(1)D中除硝基外还含有的官能团的名称__________。D生成E的反应类型是________。
(2)鉴别A和E可用的试剂是__________________。
a.氢氧化钠溶液 b.氯化铁溶液
c.碳酸氢钠溶液 d.浓溴水
(3)反应①、③的作用____________________。
(4)写出反应⑤的化学方程式___________________。
写出F与过量NaOH共热时反应的化学方程式_________________。
(5)B有多种同分异构体,写出符合下列条件的一种物质的结构简式
①只有一种官能团
②能发生银镜反应
③苯环上的一氯取代物只有二种
④核磁共振氢谱共有四组峰,峰面积之比为3 :2 :2 :1
A.【化学—选修3.物质结构与性质】周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族,e的最外层只有1个电子,但次外层有18个电子。请填写下列空白。
(1)e元素基态原子的核外电子排布式为_____________。
(2)b、c、d三种元素的第一电离能数值由小到大的顺序为___________(填元素符号),其原因是____________。
(3)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为___________________;分子中既含有极性共价键,又含有非极性共价键的化合物是______________(填化学式,写出两种)。
(4)已知c、e能形成晶胞如图甲和图乙所示的两种化合物,化合物的化学式为分别为:甲________________,乙___________;甲高温易转化为乙的原因是______________。
(5)这5种元素形成的一种1 :1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图丙所示)。该化合物中,阴离子为_______________,该化合物加热时首先失去的组分是______________,判断理由是________________