PC是一种可降解的聚碳酸酯类高分子材料,由于其具有优良的耐冲击性和韧性,因而得到了广泛的应用。以下是某研究小组开发的生产PC的合成路线: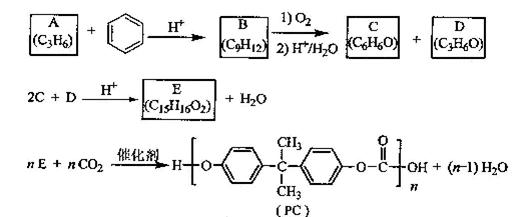
已知以下信息:
①A可使溴的CCl4溶液褪色;
②B中有五种不同化学环境的氢;
③C可与FeCl3溶液发生显色反应:
④D不能使溴的CCl4褪色,其核磁共振氢谱为单峰。
请回答下列问题:
(1)A的化学名称是 ;
(2)B的结构简式为 ;
(3)C与D反应生成E的化学方程式为 ;
(4)D有多种同分异构体,其中能发生银镜反应的是 (写出结构简式);
(5)B的同分异构体中含有苯环的还有 种,其中在核磁共振氢谱中出现丙两组峰,且峰面积之比为3:1的是 (写出结构简式)。
为比较温室效应气体对全球增温现象的影响,科学家以CO2为相对标准,引入了“温室效应指数”的概念(如下表)。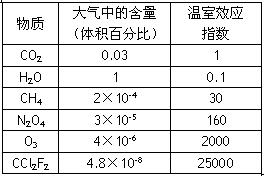
回答下列问题:
⑴6种气体中,温室效应指数最大的物质属于 ▲(选填“极性分子”或“非极性分子”)。
⑵在水分子中,O原子上的价层电子对数为 ▲。
⑶N2O4分子结构式为 ,分子为平面结构。N2O4分子中N原子的杂化方式为 ▲,在N2O4分子的结构式上,将你认为是配位键的共价键上加上箭头 ▲。
,分子为平面结构。N2O4分子中N原子的杂化方式为 ▲,在N2O4分子的结构式上,将你认为是配位键的共价键上加上箭头 ▲。
⑷O3具有吸收紫外光的功能。
①根据等电子原理,判断O3分子的空间构型为 ▲。
②紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因: ▲。
| 共价键 |
C-C |
C-N |
C-S |
| 键能/ kJ·mol-1 |
347 |
305 |
259 |
已知A、B、C、D、E、F均为周期表中前36号元素,且原子序数依次增大。A、B、C为同一周期的主族元素,B原子p能级电子总数与s能级电子总数相等。A、F原子未成对电子是同周期中最多的,且F基态原子中电子占据三种不同形状的原子轨道。D和E原子的第一至第四电离能如下表所示:
| 电离能/ kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
| D |
738 |
1451 |
7733 |
10540 |
| E |
578 |
1817 |
2745 |
11578 |
⑴A、B、C三种元素的电负性最大的是 ▲(填写元素符号),D、E两元素中D的第一电离能较大的原因是 ▲。
⑵F基态原子的核外电子排布式是 ▲;在一定条件下,F原子的核外电子从基态跃迁到激发态产生的光谱属于 ▲光谱(填“吸收”或“发射”)。
⑶根据等电子原理,写出AB+的电子式: ▲。
⑷已知:F3+可形成配位数为6的配合物。组成为FCl3·6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3∶2∶1。则绿色配合物的化学式为 ▲。
A.[CrCl (H2O)5]Cl2·H2O B.[CrCl2(H2O)4]Cl·2H2O
C.[Cr(H2O)6]Cl3D.[CrCl3(H2O)3] ·3H2O
自然界钨主要以钨(+6)酸盐的形式存在,黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4)。黑钨矿传统冶炼工艺流程图如下:
⑴写出上述第一步转化中生成MnO2的化学反应方程式 ▲;整个转化过程中黑钨矿被氧化的元素是 ▲。
⑵检验沉淀C是否洗涤干净的操作是 ▲。
⑶已知上述转化中W的化合价未发生变化,将产品D用碳或氢气还原均可得到钨,根据实际生产需要,请你选择合适的还原剂,说明理由: ▲。
⑷产品D有一种蓝色非整比的存在形态,其化学式为WO3-x,该化合物中存在五价和六价两种价态的钨。若x=0.1,则化合物中五价和六价的钨原子数之比为 ▲。
某有机化合物A的结构简式如图回答下列问题:
(1)A在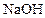 水溶液中加热得到B和C,C 是芳香族化合物,则C的结构简式是。
水溶液中加热得到B和C,C 是芳香族化合物,则C的结构简式是。
(2)C酸化后可得F,F不能发生的反应类型是(填写字母代号)。
a.取代反应 b.加成反应 c.消去反应
d.加聚反应 e.氧化反应 f.还原反应
(3)B与足量的某饱和一元羧酸D充分反应后生
成E,E和B的相对分子质量之差为84,则D的摩尔质量为。
(4)F可以发生如下转化,且G与H互为同分异构体。
请写出:①H的结构简式。②由F生成G的化学方程式。
(5)符合下列三个条件的F的同分异构体的数目有多种,任写出其中一种的结构简式。
①含有邻二取代苯环结构②与F具有相同的官能团③不与 溶液发生显反应
溶液发生显反应
具有水果香味的中性物质A可以发生下列变化: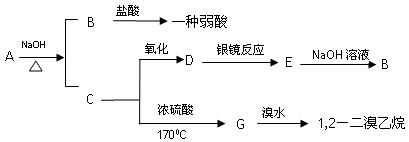
(1)推断下述物质的名称
A ___________、B _________。
(2)写出下列变化的化学方程式:
A与NaOH溶液反应 ___________________________________________ ;
D的银镜反应 _________________________________________________ 。