碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置)
请回答下列问题。
(1)气体X的主要成分有______ ______。(写化学式)
______。(写化学式)
(2)洗 气瓶中的反应现象为_____________。用文字简要解释产生上述实验现象的原因:_______________________。
气瓶中的反应现象为_____________。用文字简要解释产生上述实验现象的原因:_______________________。
(3)管口Z处的现象是_________________,产生此现象的原因是_______________。(用化学方程式表示)
某工厂废液中含有氯化钠.氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如下图所示,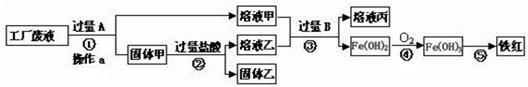
回答下列问题。
(1)固体甲_______,操作a的名称是_______。
(2)工厂废液中加入过量A反应的化学方程式为 。
(3)溶液甲中的金属离子是 (写离子符号)。
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是 (填序号)。
某化学兴趣小组的同学利用如图所示的装置验证Na2CO3样品的纯度(样品中的杂质与稀盐酸不反应),小资料:无水CaCl2可作干燥剂,与CO2不反应。
(1)有关反应的化学方程式为______。
(2)装置中的“无水CaCl2”的作用是______。
(3)若反应前,称量整个装置及药品的总质量为598.6g,其中样品质量为6g;打开分液漏斗向广口瓶中加入足量的稀盐酸,充分反应后,应该进行的操作是______,然后再第二次称量整个装置及药品的总质量为596.4g,则该样品的纯度为(样品中碳酸钠的质量分数)为_________。
A~F为初中化学常见物质,它们由H、C、O、Cl、Na、Ca中的元素组成。
(1)A为氧化物,可用于制备改良酸性土壤的碱,写出用A制备碱的化学方程式 。
(2)B、C均为液体,且组成元素相同,C在一定条件下可生成B,B的化学式为 。
(3)D用于玻璃、造纸、纺织、洗涤剂的生产。
取D溶液进行实验,操作及部分现象如图所示。D与F反应的化学方程式为 。
(4)从上述物质中任选2种为一组,按下图装置进行实验,将液体滴入瓶中,关闭活塞。请根据表中现象,写出符合要求的物质。
| 现象 物质 |
气球变鼓,一段时间后恢复原状 |
气球变鼓,一段时间后不恢复原状 |
| 液体 |
||
| 固体 |
某研究性学习小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)。查阅资料:CO2 + Zn  CO + ZnO;FeCl3溶液遇KSCN溶液变红。
CO + ZnO;FeCl3溶液遇KSCN溶液变红。
请回答下列问题:
(1)仪器A的名称是 ,装置B的作用是 ,尾气处理的方法是 。
(2)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D进行加热,其产物均为黑色粉末(纯净物)。两组分别用产物进行以下实验:
| 步骤 |
操作 |
甲组现象 |
乙组现象 |
| 1 |
取黑色粉末加入盐酸 |
溶解,无气泡,溶液呈浅黄绿色(含两种金属离子) |
溶解,有气泡,溶液呈浅绿色 |
| 2 |
取步骤1所得溶液,滴加KSCN溶液 |
变红 |
无现象 |
则甲组步骤1中反应的化学方程式是 ,乙组得到的黑色粉末是 。
(3)从安全考虑,本实验应在装置 和 之间添加装置E防止倒吸。(填字母编号)
(4)该对比实验结果表明CO的还原能力随温度的升高而 (填“增强”或“减弱”)。
课外小科约老师继续探究铁粉和硫粉反应的实验:他们各自取一定量的铁粉和硫粉均匀混合后堆放在石棉网上,在其中插入烧红的玻璃棒,反应立即发生。拿掉玻璃棒后,反应继续剧烈进行,反应过程中有少量刺激性气味的气体x产生。反应结束后,都得到了黑色固体。老师得到的黑色固体不会被磁铁吸引,而小科的却会被磁铁吸引。
(1)铁和硫的反应是 (填“放热”或“吸热”)反应。
(2)气体x的化学式为 。
(3)对比老师的实验结果,小科猜想自己得到的黑色固体可能是有剩余的铁或有生成的四氧化三铁。小科想验证是否有铁剩余。
老师启发小科:硫化亚铁能与稀硫酸反应,产生硫化氢气体,该气体能被氢氧化钠溶液吸收。于是,小科认为正确连接如图所示的三个装置并进行实验,如果a处有水压出,就能验证有铁剩余。
①小科依次连接各装置的导管口:e→ →b→a。(填“c→d”或“d→c”)
②老师指出设计不够合理,不能就此验正猜想。请你帮小科说出不够合理的原因: 。
于是小科改进了实验设计,继续进行探究…