现有浓度均为0.1 mol/L的下列溶液:①硫酸 ②醋酸 ③氢氧化钠
④氯化铵 ⑤醋酸铵 ⑥硫酸铵 ⑦硫酸氢铵 ⑧氨水,请回答下列问题:
(1)①②③④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_ 。
(2)④⑤⑥⑦⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)___ ___。 (3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是 _____。
(3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是 _____。
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”) 25℃。在t℃时将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b= 。
(5)25℃时,有pH=x的盐酸和pH="y" 的氢氧化钠溶液(x≤6,y≥8),取aL该盐酸与该氢氧化钠溶液中和,消耗bL的氢氧化钠溶液,问:
①若x+y=14,则a/b=__ __(填数据);②若x+y=13,则a/b=__ __
(填数据);
③若x+y>14,则a/b=__ __(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的pH x和y的关系式 (填表达式)。
(6分)下表是某地市场上销售的一种“加碘盐”包装袋上的部分文字说明。请根据此表,结合初中学过的化学知识,回答下列问题:
| 配料表 |
精制海盐、碘酸钾(KIO3) |
| 含碘盐 |
20~40mg/kg |
| 储藏方法 |
密封避光、防潮 |
| 使用方法 |
烹调时待食品熟后加入碘盐 |
(1)碘酸钾属于哪类物质?______________(填:“纯净物”、“混合物”、“单质”、“氧化物”)
(2)根据含碘盐的食用方法,可推测碘酸钾的化学性质:
碘酸钾在受热时_____________。
(3)我国规定,食盐含碘量为每千克食盐含碘0.035g,相当于每千克食盐含碘酸钾 g (结果保留三位小数)。
(8分)下列物质中,物质的量最大的是 ,含分子个数最多的是 ,含原子个数最多的是 ,质量最大的是。(填字母)
A 6g氢气 B 0.5mol CO2 C 1.204×1024个氯化氢分子D、147g硫酸
E、92g乙醇(C2H5OH) F、4℃9 mL水
[化学——选修3:物质结构与性质](15分)前四周期原子序数依次增大的元素A、B、C、D中A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
回答下列问题:
(1)D2+的价层电子排布图为。
(2)四种元素中第一电离能最小的是,电负性最大的是。
(填元素符号)
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。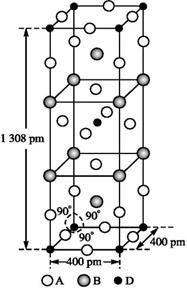
①该化合物的化学式为,D的配位数为;
②列式计算该晶体的密度g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有;
(5)该化合物中存在一个复杂离子,该离子的化学式为,配位体是。
(1)25℃时,在0.10mol/L的氨水中逐滴加入同浓度的盐酸(不计两者的挥发性),回答下列问题:
①当溶液pH=7时,溶液中c(NH4+)c(Cl-)(用“<”、“>”、“=”填空,下同);
②当盐酸和氨水溶液恰好中和时,溶液中c(H+)c(OH-);
(2)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。某实验小组的同学对该厂生产的印刷电路后所得的废液进行了分析:取50mL废液,向其中加入足量的稀硝酸,生成0.02molNO;另取50mL废液,向其中加入足量的AgNO3溶液,析出沉淀43.05g。
请回答以下问题:
①该厂原来使用的FeCl3溶液中溶质的物质的量浓度为_____(反应前后溶液的体积变化忽略不计);
②废液中各金属阳离子的物质的量浓度之比为C(Fe3+):C(Fe2+):C(Cu2+)=__________;
③另取50mL废液,加入一定量铁屑,充分反应后有铜析出,则所得溶液中Fe2+的物质的量范围是。
X、Y、Z、W、V是原子序数依次增大的短周期主族元素,其中两种为金属元素。Y的原子半径是短周期主族元素中最大的,Z的单质可与Y的最高价氧化物的水化物溶液反应,X与W同主族,且W的原子序数是X的两倍。请回答下列问题:
(1)W的氢化物的电子式是,其相对分子质量与H2O2的相对分子质量相等,但其沸点却低于H2O2的沸点,可能的原因是_________________________;
(2)Z的单质与Y的最高价氧化物的水化物溶液溶液反应的离子方程式是______________;
(3)X与W以原子个数比2∶1形成的化合物能使溴的水溶液褪色,写出反应的离子方程式__________,该化合物表现了性;
(4)V的单质溶于水后形成的溶液中存在的粒子有种。