用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出反应的离子方程式。
(1)FeSO4(CuSO4):
所需试剂(填化学式) ,所涉及的离子方程式: 。
(2)O2(CO2):
所需试剂(填化学式) ,所涉及的离子方程式: 。
(14分)迷迭香酸(F)的结构简式为:
它是存在于许多植物中的一种多酚,具有抗氧化、延缓衰老、减肥降脂等功效。以A为原料合成F的路线如下(已知苯环上的羟基很难直接与羧酸发生酯化反应):
根据题意回答下列问题:
(1)A的结构简式为___________;反应②的反应类型是___________。
(2)反应③的试剂为___________。
(3)1mol F分别与足量的溴水和NaOH溶液反应,最多可消耗Br2mol、NaOHmol。
(4)E在一定条件下发生缩聚反应的化学方程式是。
(5)与E互为同分异构体,且同时满足下列条件的有机物有_____________种。
①苯环上有四个取代基,且苯环上的一氯取代物只有一种。
②1 mol该物质分别与NaHCO3、Na2CO3反应时,最多消耗NaHCO3、Na2CO3的量分别是1 mol和4mol。
已知:乙二酸(HOOC-COOH,可简写为H2C2O4),俗称草酸,157℃时开始分解。
(1)探究草酸的酸性
25℃H2C2O4 K1 = 5.4×10-2,K2= 5.4×10-5;H2CO3 K1=4.5×10-7 K2= 4.7×10-11
下列化学方程式可能正确的是。
| A.H2C2O4 + CO32- = HCO3- + HC2O4- |
| B.HC2O4- + CO32- = HCO3- + C2O42- |
| C.2C2O42- + CO2 + H2O = 2HC2O4- + CO32- |
| D.H2C2O4 + CO32- = C2O42- + H2O +CO2↑ |
(2)探究草酸分解产物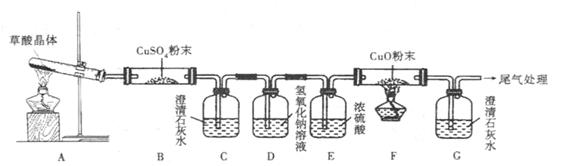
实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用是,证明有CO气体生成的现象是。
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入4mL 0.01mol/L KMnO4酸性溶液2mL 0.1mol/L H2C2O4溶液, 再向乙试管中加入一粒黄豆大的MnSO4固体,摇匀。填写下表:
| 反应现象 |
|
| 实验结论 |
|
| 试管中发生反应的离子方程式 |
(4)用酸性KMnO4溶液滴定Na2C2O4,求算Na2C2O4的纯度
实验步骤:准确称取2.0g Na2C2O4固体,配成100mL溶液;取出20.00mL于锥形瓶中,再向瓶中加入足量稀H2SO4;用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。
① 高锰酸钾溶液应装在_______滴定管中。(填“酸式”或“碱式”)
②Na2C2O4的纯度是______________。
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。
(1)双氧水的电子式为;Ⅰ中发生反应的还原剂是(填化学式)。
(2)Ⅱ中反应的离子方程式是。
(3)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备。
①写出该反应的化学方程式:;
②研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析,其原因是。
(4)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量(填“相同”、“不相同”或“无法判断”)
(10分)铜及其化合物在工农业生产及日常生活中应用非常广泛。
(1)由辉铜矿制取铜的反应过程为:
2Cu2S(s) + 3O2 (g) = 2Cu2O(s) + 2SO2(g)△H=-768.2kJ·mol-1,
2Cu2O(s) + Cu2S(s) =" 6Cu(s)" + SO2(g)△H=+116.0kJ·mol-1,
请写出Cu2S与O2反应生成Cu与SO2的热反应方程式:。
(2)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl-) 的关系如图。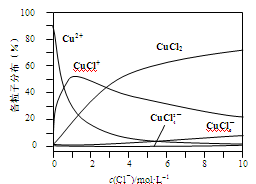
①当c(Cl-)="9" mol·L-1时,溶液中主要的3种含铜物种浓度大小关系为。
②在c(Cl-)="1" mol·L-1的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的离子方程式为(任写一个)。
(3) 电解Na2HPO3溶液可得到亚磷酸,装置如下图(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过)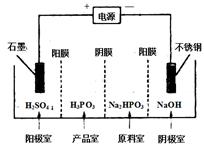
①阳极的电极反应式为:____________。
②产品室中反应的离子方程式为:_____。
(Ⅰ)硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
①BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H=+ 571.2 kJ・mol—1
②BaS(s)=Ba(s)+S(s)△H=+460 kJ・mol—1
已知:③2C(s)+O2(g)=2CO(g)△H=" -221" kJ・mol—1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s)△H=。
(Ⅱ)污染与环境保护已经成为现在我国最热门的一个课题,污染分为空气污染,水污染,土壤污染等。
(1)为了减少空气中SO2的排放,常采取的措施就洗涤含SO2的烟气。以下物质可作洗涤剂的是(选填序号)。
a.Ca(OH)2b.CaCl2c.Na2CO3d.NaHSO3
(2)为了减少空气中的CO2,目前捕碳技术在降低温室气体排放中具有重要的作用,捕碳剂常用(NH4)2CO3,反应为:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3 (aq)ΔH3为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,其关系如图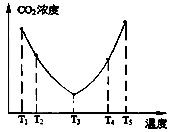
则:
①△H30(填“>”、“=”或“<”)。
②在T4~T5这个温度区间,容器内CO2气体浓度变化趋势的原因是:。
(3)催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
①催化反硝化法中,用H2将NO3-还原为N2,一段时间后,溶液的碱性明显增强。则反应离子方程式为:。
②电化学降解NO3-的原理如图,阴极反应式为:。