写出下列有机物的结构简式:
(1)2,6-二甲基-4-乙基辛烷: ;
(2)2-甲基-1-戊烯: ;
(3)有A、B、C三种烃,它们的结构简式如下图所示: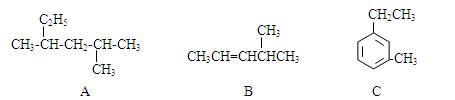
A的名称是 ;B的名称是 ;
C的名称是 。
可逆反应:aA(g)+ bB(g) cC(g)+ dD(g);根据图回答:
cC(g)+ dD(g);根据图回答:
(1)压强 P1比P2(填大或小);
(2)(a +b)比(c +d)(填大或小);
(3)温度t1℃比t2℃(填高或低);
(4)正反应为反应。
在密闭容器中进行可逆反应: CO(气)+NO2(气)  CO2(气)+NO(气) △H<0,达到平衡后,只改变其中一个条件,对平衡的影响是:
CO2(气)+NO(气) △H<0,达到平衡后,只改变其中一个条件,对平衡的影响是:
(1)增大容器的体积,平衡 ,反应混合物的颜色 。
(2)通人CO2气体,平衡 ,反应混合物的颜色 。
(3)加入催化剂,平衡 。
二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等领域也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳。
Ⅰ.①氧化产物是
②请写出化学反应方程式,并用双线桥法表示该反应的电子转移总 数
数
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示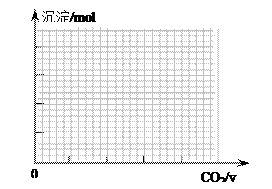
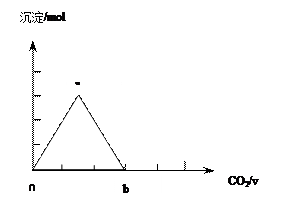
写出沉淀变化由a到b的离子方程式:
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系; 并写出与上图中不同曲线处对应的离子反应方程式 ;
并写出与上图中不同曲线处对应的离子反应方程式 ;
。

已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化 物A起反应。
物A起反应。
据此,请填空:
⑴化合物F的化学式为__________,化合物I的化学式为_____________,氧化物A的晶体类型为_____________。
⑵反应①的化学方程式为___________________________________。
⑶氧化物A与烧碱溶液反应的离子方程式为___________________________________。
三氟化氮是一种无色、无味、无毒且不可燃的气体,可在铜的催化作用下由F2和过量NH3反应得到,在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO 和 HNO3,请根据要 求回答下列问题:
求回答下列问题:
⑴写出制备NF3的化学反应方程式:。反应过程中,氧化剂与还原剂的物质的量之比为。
⑵写出三氟化氮与水蒸气反应的化学方程式:。⑶NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体
泄漏时的现象是。
⑷一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染。其产物除H2O外,还有另三种
钠盐:(填化学式)。