某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。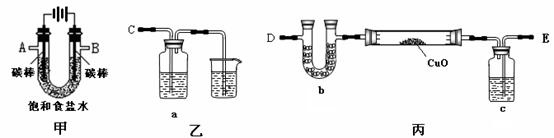
(1)为完成上述实验,正确的连接顺序为A连_______;B连_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜 粉末加热前,需要的操作为________________。
粉末加热前,需要的操作为________________。
(3)若检验 氯气的氧化性,则乙装置的a瓶中溶液可以是_____________,对应的现象为___________________________________________________。
氯气的氧化性,则乙装置的a瓶中溶液可以是_____________,对应的现象为___________________________________________________。
(4)丙装置的c瓶中盛放的试剂为 _____________,作用是____________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案
精确测量硬质玻璃管的质量为a g,放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g,实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
①请你分析并回答:________方案测得结果更准确。你认为不合理的方案的不足之处在________________________________。
②按测得结果更准确的方案进行计算,Cu的相对原子质量___________________。
某化学研究性学习小组设计制取氯气及探究其性质的方案,并按下图所示装置完成实验。(A中发生反应的化学方程式为:MnO2 + 4HCl(浓) ==== MnCl2 + Cl2↑ + 2H2O)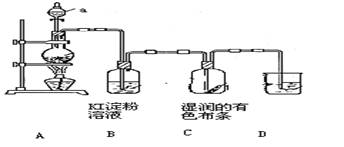
【实验探究】
(1)装置A中,仪器a的名称是。
(2)装置B中无色溶液将变为色,该反应的化学方程式是。
(3)装置C中湿润的有色布条(填“褪色”或“不褪色”),其原因是氯气与水反应生成了(填化学式)
(4)为了吸收多余的氯气,防止造成空气污染,装置D中应盛放 ____溶液(填“NaOH”或“H2SO4”)
(5)用8.7gMnO2与足量浓盐酸反应,理论上可以生成标准状况下的Cl2_______L。
【知识拓展】
(6)某同学查阅资料得知:高锰酸钾与浓盐酸在常温下也可以生成氯气(反应的化学方程式为:
2KMnO4 + 16HCl(浓) ="===" 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O),该反应的氧化剂是(填“KMnO4”或“HCl”)
【知识应用】
(7)洪灾过后,饮用水的消毒杀菌是抑制大规模传染疾病爆发的重要措施之一。请你列举一例对饮用水进行消毒杀菌的合理方法:______________________________________________________________________
实验室要配制480 mL 0.2 mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有__________________(填选项的字母)。
A.烧杯B.500 mL容量瓶 C.漏斗 D.胶头滴管E.玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为_______________g。
(3)取用任意体积的该NaOH溶液时,下列物理量中不随所取体积的多少而变化的是_______。
A.溶液中NaOH的物质的量 B.溶液的浓度
C.溶液中OH-的数目 D.溶液的密度
(4)在配制上述溶液的过程中,下列情况对 NaOH溶液物质的量浓度有何影响(填“偏高”、“偏低”、或“无影响”)
①未经冷却趁热将溶液注入容量瓶中:______________
②容量瓶用蒸馏洗涤后残留有少量的水:_____________
③定容时某同学观察液面的情况如图所示,则所配制的溶液的浓度____________。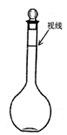
④转移溶液后,未洗涤烧杯和玻璃棒就直接定容___________。(“偏低”、或“无影响”)
亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。
已知:室温下,①2NO+Na2O2 = 2NaNO2
②3NaNO2+3HCl ="=" 3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式。
(2)B中观察到的主要现象是有无色气体产生和,D装置的作用是。
(3)检验C中产物有亚硝酸钠的方法是。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称。
(5)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭g。
(1)玻璃棒是中学化学实验中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是。(填写编号)
①粗盐提纯
②配制一定物质的量浓度的氯化钠溶液
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
④探究Ba(OH)2·8H2O晶体和NH4Cl晶体反应过程中的能量变化
⑤实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
(2)实验室欲配置450mL0.25mol·L-1NaOH溶液:
①配制时除需用胶头滴管、托盘天平(带砝码)、玻璃棒、药匙外,还必需用到的仪器是。
②通过计算,应用托盘天平称取NaOH固体,若将物码放反,则所配制溶液物质的量浓度。(填“偏大”、“偏小”或“不变”)
③定容时,仰视液面,则所配溶液物质的量浓度。(填“偏大”、“偏小”或“不变”)
氯气是一种重要的工业原料.
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是.
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:
Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O
2CaSO4+2Cl2↑+2H2O
他们利用该反应设计如下制取氯气并验证其性质的实验.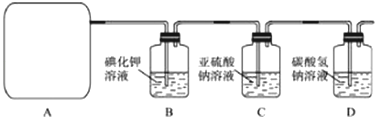
回答下列问题:
(1)该实验中A部分的装置是(填标号).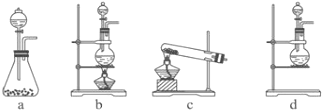
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):.
(3)写出D装置中发生反应的离子方程式.
(4)该实验存在明显的缺陷,请你提出改进的方法.
(5)该小组又进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置.待完全反应后,用0.1mol•L﹣1的Na2S2O3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI,共用去Na2S2O3溶液20.0mL.则该漂白粉中Ca(ClO)2的质量分数为.