一定条件下,在体积为3L的密闭容器中,CO与H2反应生成甲醇(催化剂为Cu2O/ZnO):CO (g) + 2H2 (g)  CH3OH (g)
CH3OH (g)
根据题意完成下列各题: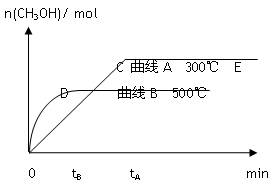
(1)反应达到平衡时,平衡常数表达式K="_________________ " 升高温度,K值___________ (填“增大”、“减小”或“不变”)
(2)在500℃,从反应开始到平衡,H2的平均反应速率v (H2) =" ___________"
(3)在其它条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列说法正确的是__________
a. H2的浓度减少 b. 正反应速率加快,逆反应速率也加快
c .甲醇的物质的量增加 d. 重新平衡时n (H2) / n (CH3OH)增大
(4)据研究,反应过程中起催化作用的是Cu2O,反应体系中含有少量CO2有利于维持催化剂Cu2O的量不变,原因是________________(用化学方程式表示)
在一定条件下的下列可逆反应达到平衡时,试填出:xA+yB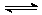 zC
zC
⑴ 若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、 y、z关系是_____________;若只有A是
y、z关系是_____________;若只有A是 有色物质,反应混合物的颜色(变深、变浅或不变)。
有色物质,反应混合物的颜色(变深、变浅或不变)。
⑵ 若C是气体,并且x+y=z,在加压时化学平衡可发生移动,则平衡必定是向_____方向移动;
⑶ 已知B、C是气体,现增加A物质的量,平衡不移动,说明A是____________(填状态);
⑷ 如加热后 ,C的百分含量减小,则正反应是________热反应。
,C的百分含量减小,则正反应是________热反应。
潜艇的金属外壳浸在海水中,在海水和空气的作用下会 被腐蚀
被腐蚀
(1)若海水呈中性,一艘钢制外壳的潜艇在海水中发生腐蚀的电极反应式为:
正极:___________________________________________________________ ______ _,负极:__________________________________________________________。
______ _,负极:__________________________________________________________。
(2)为有效地保护潜艇。下列措施中最好的是______________(填序号)
| A.采用纯铁制造潜艇外壳 | B.采用耐腐蚀的合金制造潜艇外壳 |
| C.在潜艇上涂一层油 | D.在潜艇外壳上装一定数量的锌块 |
A、B、C、D4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的 原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称________;B在周期表中的位置第______周期,第________族;
(2)A、B形成的化合物的电子式________;
(3)C的元素符号________,C的最高价氧化物的化 学式________;
学式________;
(4) D的最高价氧化物对应的水化物的化学式________.
下列是用化学方程式表示的化学变化,请在每小题后的横线上注明能量的转化形式。
(1)Zn+Ag2O+ H2O Zn(OH)2+2Ag;(正反应过程)_____________
Zn(OH)2+2Ag;(正反应过程)_____________
(2)2C2H2+5O2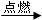 4CO2+2H2O; ______________
4CO2+2H2O; ______________
(3) ; _____ _________
; _____ _________
(4)CaCO3 CaO+CO2↑;_____ _________
CaO+CO2↑;_____ _________
某气态烷烃和乙烯等体积混合时,1体积混合气体完全燃烧消耗同温同压下4.75体积氧气。试回答:
(1)该烷烃的分子式为;
(2)该烷烃所有同分异构体的结构简式为。