将Fe粉、Cu粉、FeCl3溶液、FeCl2和CuCl2溶液,混合于某容器中充分反应(假定容器不参与反应),试判断下列情况下溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能 ;
(2)若氯化铜有剩余,则容器中还可能有 ;
(3)若氯化铁和氯化铜都有剩余,则容器中不可能有 , 可能有 。
(4)若氯化铁有剩余,则容器中不可能有 。
(1)请指出下列做法中分别应用了哪些分离方法?(过滤、蒸发、蒸馏 、萃取、结晶)
a、熬煮中药__________________ b、分离豆浆和豆渣__________________
c、用海水晒盐____________________ d、海水淡化__________________
(2)写出离子反应方程式H+ + OH- =H2O所对应的两个不同类型化学方程式
①
②
(3).在下列反应中:
| A.2F2+2H2O=4HF+O2 | B.2Na+2H2O=2NaOH+H2↑ |
| C.CaO+H2O=Ca(OH)2 | D.2H2O=2H2↑+O2↑ |
水只作氧化剂的是,水只作还原剂的是,水既作氧化剂又作还原剂的是,水既不作氧化剂又不作还原剂的是。请用线桥表示B反应的电子转移方向和数目。
2Na+2H2O=2NaOH+H2↑
(1)0.5L 0.5mol/L FeCl3溶液中的Cl-的物质的量浓度为 __________。
(2)在mL 0.2 mol/L NaOH溶液中含1 g溶质;配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4·5H2O g。
(3)中和相同体积、相同物质的量浓度的NaOH溶液,并使其生成正盐,需要相同物质的量浓度的盐酸、硫酸、磷酸溶液的体积比为。
(4 )今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、H+、Mg2+、Ba2+、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加入足量NaHCO3溶液后,收集到气体0.03mol。
②第二份加足量Ba(NO3)2溶液充分反应后过滤干燥,得干燥沉淀4.66g。
根据上述实验回答:
(a)原溶液中一定不存在的离子是_______________________。
(b)原溶液中可能存在的离子是_______________________。
(c)请计算出原溶液中一定存在的阴离子的物质的量浓度________________。
“滔滔”是我国第一例转入人体白蛋白基因的转基因试管牛,人们利用该转基因奶牛的乳汁能生产人类血清白蛋白。
(1)试管动物实际上是体外受精与胚胎移植两项技术的综合运用。体外受精前需要对奶牛的精子进行_________处理,方法是将精子放入一定浓度的_________或钙离子载体A23187溶液中。防止多精入卵的生理反应包括______________和________________。胚胎工程的终端环节是胚胎移植。移植后的胚胎能在受体子宫内存活的生理基础是___________________________________。
(2)人体白蛋白基因通常可以从基因文库中获取,含有一种生物所有基因的文库称为____________,获得人体白蛋白基因后可以利用________技术进行扩增。基因工程的核心步骤是______________________________。人体白蛋白基因一般利用____________技术导入牛的受精卵中,当受精卵分裂到囊胚期时,需要取囊胚的____________细胞进行性别鉴定,以确保发育成熟的牛能分泌乳汁。
现在大力提倡无纸化办公,但是仍然不可避免的每年要产生大量的废纸,其主要成分是木质纤维,人类正努力将其转化为一种新的资源——乙醇。右图是工业上利用微生物由纤维素生产乙醇的基本工作流程,请回答相关问题: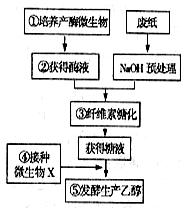
(1)自然界中①环节需要的微生物大多分布在
________________________的环境中。将从土壤中获得的微生物培养在以______________为碳源、并加入__________的培养基上筛选周围有___________的菌落。
(2)如上所述的筛选中获得了三个菌落,对它们分别培养,并完成环节②,且三种等量酶液中酶蛋白浓度相同,则你认为三种酶液的活性___________(一定相同、不一定相同、一定不同),可以通过对_______________________进行定量测定来验证。
(3)根据测定结果,①环节常选择木霉,则②中获得的酶是_____________酶。该酶至少包括__________、____________、________________三个组分。
(4)生产中可以满足④环节的常见菌种是___________,为了确保获得产物乙醇,⑤环节要注意_______________,④过程要注意避免________________________。
下图为蛋白质合成示意图(图中甲表示甲硫氨酸,丙表示丙氨酸),请据图分析:
(1)该图表示__________过程,组成②的单体是______________。
(2)丙氨酸的密码子是_________。若合成的蛋白质由570个氨基酸组成,那么与③对应的基因中有___________对碱基。
(3)图中④表示甲和丙之间的结合方式是_____________,甲和丙之间的化学键结构式是_____________。
(4)若③上的某一个碱基发生了改变,不一定引起相应的氨基酸的改变,因为____________________________________________________。
(5)该过程不可能发生在人的( )
| A.神经细胞 | B.肝细胞 | C.成熟的红细胞 | D.脂肪细胞 |