开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的。
Ⅰ.由C、H、O三种元素中的两种和三种分别组成的燃料物质甲和乙,其分子中均有氧,且1个乙分子中含有18个电子,则甲和乙分别是________。乙是一种清洁燃料,工业上可用甲和氢气反应制得。
(1)T1温度时,在体积为2 L的密闭容器中充入2 mol甲和6 mol H2,反应达到平衡后,测得c(甲)=0.2 mol/L,则乙在平衡混合物中的物质的量分数是 。
(2)升高温度到T2时,反应的平衡常数为1,下列措施可以提高甲的转化率的是________(填字母)。
A.加入2 mol甲 B.充入氮气
C.分离出乙 D.升高温度
Ⅱ.(1)甲烷也是一种清洁燃料,但不完全燃烧时热效率降低并会产生有毒气体造成污染。
已知:①CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH1=―890.3 kJ/mol
②2CO (g) + O2(g) = 2CO2(g) ΔH2=―566.0 kJ/mol
则甲烷不完全燃烧生成一氧化碳和液态水时的热效率只是完全燃烧时的________倍(计算结果保留1位小数)。
(2)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol/L的氯化铜溶液的装置示意图:
请回答:
①若使用酸性水溶液做电解质,甲烷燃料电池的负极反应式是________。
若使用熔融Na2CO3做电解质,该电池负极的反应式是 。
若使用燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,可以传导O2—。则在电池内部O2—由____极移向____极(填“正”或“负”);电池的负极电极反应式为 。
②若B中为氯化铜溶液,当线路中有0.1 mol电子通过时,________(填“a”或“b”)极增重________g。
若B中为足量Mg(NO3) 2和NaCl的混合溶液。电解开始后阴极的现象为____ 。
对于溶液中进行的反应:FeCl3+3KSCN===Fe(SCN)3+3KCl,当其他条件一定时:
(1)向溶液中加入少量的KCl固体,溶液的颜色_______
(2)向溶液中加入少量KSCN固体,溶液的颜色_______
(3)加水稀释时,化学平衡向_______移动
在密闭容器中,当合成氨的反应N2+3H2===2NH3(正反应是放热反应)达到平衡时,改变如下的一些条件:
| A.升温, | B.加压, | C.减压, | D.增大c(H2),(E)减小c(NH3),(F)增大c(NH3),若平衡向右移动用“ →”,若平衡向左移动用“←”表示;若值增加用“↑”表示,若值减小用“↓”表示,请根据下表中各项的变化情况,在改变条件栏目中填上相应的编号(每项只改变一个条件)。 |
| 编号 |
改变条件 |
平衡移动方向 |
N2的转化率 |
C(NH3) |
C(N2) |
C(H2) |
| ① |
→ |
↑ |
↓ |
↓ |
↓ |
|
| ② |
← |
↓ |
↓ |
↑ |
↑ |
|
| ③ |
→ |
↑ |
↑ |
↓ |
↑ |
|
| ④ |
← |
↓ |
↓ |
↓ |
↓ |
|
| ⑤ |
→ |
↑ |
↑ |
↑ |
↑ |
对于反应:2SO2+O2===2SO3,当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格里(填“增大”、“减小”或“不变”)
| 编号 |
改变的条件 |
生成SO3的速率 |
| ① |
升高温度 |
|
| ② |
恒压下充入Ne |
|
| ③ |
增大O2的浓度 |
|
| ④ |
使用催化剂 |
|
| ⑤ |
压缩体积 |
|
| ⑥ |
恒容下充入Ne |
下图是利用石油为原料合成增塑剂G的基本流程: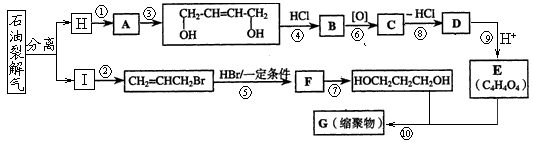
请完成下列各题:
(1)反应⑧条件是。
(2)写出反应⑦的化学方程式:。
(3)B被氧化成C的过程中会有中间产物生成,该中间产物可能是(写出一种物质的结构简式),检验该物质存在的试剂是。
(5)写出相对分子质最小,跟E互为同系物的有机物的结构简式_________________,写出G的结构简式。
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取两种工艺品的流程如下: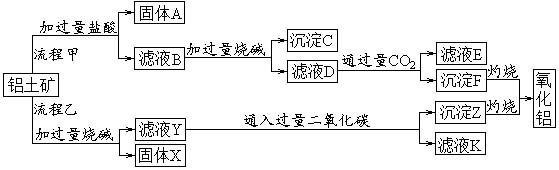
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的方程式为_________.
(2)验证滤液B含Fe3+,可取少量滤液并加入________(填试剂名称)。
(3)滤液E、K中溶质的主要成份是_____(填化学式),写出该溶液的一种用途________
(4)已知298K时,Mg(OH)2的容度积常数Ksp=5.6×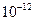 ,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=______。
,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=______。