达菲是治疗甲型H1N1流感的有效药物之一。合成达菲的原料是莽草酸,已知莽草酸和达菲的结构简式如下图所示,则有关说法中不正确的是
| A.1 mol莽草酸与足量金属钠反应最多可生成2 mol氢气 |
| B.达菲既可催化加氢,又可使酸性KMnO4溶液褪色 |
| C.达菲既可发生水解反应,又可与Br2的CCl4溶液发生加成反应 |
| D.莽草酸既可与FeCl3溶液发生显色反应,又可与NaHCO3溶液反应放出CO2 |
水热法制备直径为1~100 nm的颗粒Y(化合物),反应原理为:3Fe2+ + 2S2O32- + O2 + aOH-=" Y+" S4O62- + 2H2O,下列说法中不正确的是
| A.a=4 |
| B.将Y均匀分散到水中形成的体系具有丁达尔效应 |
| C.每有3 mol Fe2+ 参加反应,反应中转移的电子总数为5 mol |
| D.S2O32-是还原剂 |
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是 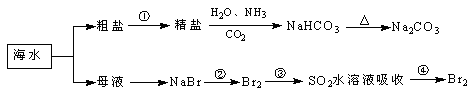
| A.工业上通过电解熔融状态MgCl2制取金属镁 |
| B.用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C.在第②、④步骤中,溴元素均被氧化 |
| D.制取NaHCO3的反应是利用其溶解度小于NaCl |
根据表中信息判断,下列选项不正确的是()
| 序号 |
反应物 |
产物 |
| ① |
KMnO4、H2O2、H2SO4 |
K2SO4、MnSO4… |
| ② |
Cl2、FeBr2 |
FeCl3、FeBr3 |
| ③ |
MnO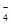 … … |
Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO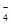 >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中不正确的是()
| A.X为直流电源的负极,Y为直流电源的正极 |
| B.阳极区pH增大 |
| C.图中的b>a |
| D.该过程中的产品主要为H2SO4和H2 |
下列说法正确的是
| A.若2H2(g)+O2(g) = 2H2O(g) ΔH=" -483.6" kJ·mol-1,则H2燃烧热为241.8 kJ·mol-1 |
| B.原子弹爆炸是放热反应 |
| C.若C(石墨,s) = C(金刚石,s) ΔH>0,则石墨能量低且键能小 |
| D.由BaSO4(s) + 4C(s) =" 4CO(g)" + BaS(s) △H1 = +571.2kJ•mol-1 ① |
BaSO4(s) + 2C(s) = 2CO2(g) + BaS(s) △H2 = +226.2kJ•mol-1 ②
可得反应C(s) + CO2(g) =" 2CO(g)" 的△H = +172.5kJ•mol-1