BAD是一种紫外线吸收剂,其合成方法如下: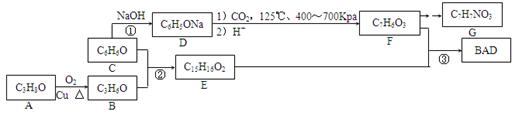
已知:
Ⅰ、B分子中所有H原子的化学环境相同;
Ⅱ、BAD的结构为: 。
。
请回答下列问题:
(1)A的名称为 。
(2)F的结构简式为 。F的一些同分异构体能使氯化铁溶液变色,能发生银镜反应,且苯环上的一硝基取代产物有两种。符合上述条件的同分异构体有 种。
(3)反应②的化学方程式为 ;反应③在一定条件下能直接进行,其反应类型为 。
(4)G是一种氨基酸,且羧基和氨基处于苯环的对位。写出G缩聚产物可能的结构简式 (只要求写一种)。
(每空1分,共7分)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答问题。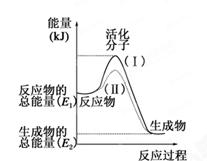
(1)图中所示反应是________(填“吸热”或“放热”)反应。
(2)已知拆开1mol H—H键、1mol I—I、1mol H—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由1mol氢气和1mol 碘反应生成HI会________(填“放出”或“吸收”)________kJ的热量。在化学反应过程中,是将______转化为________。
(3)下列反应中,属于放热反应的是________,属于吸热反应的是________。
①物质燃烧②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的碳
⑤食物因氧化而腐败⑥Ba(OH)2·8H2O与NH4Cl反应⑦铁粉与稀盐酸反应
1,4-环己二醇可通过下列路线合成(某些反应的反应物和反应条件未列出):

(1)写出反应④、⑦的化学方程式:
④________________________________; ⑦_________________________________。
(2)②的反应类型是____________,上述七个反应中属于加成反应的有____________(填反应序号)。
(3)反应⑤中可能产生一定量的副产物,其可能的结构简式为_________________。
(1)某烃A 0.2 mol在氧气中充分燃烧后,生成化合物B、C各1 mol。
①烃A的分子式为。
②若取一定量的A完全燃烧后,生成B、C各3 mol,则有g烃A参加了反应。
③若烃A不能使溴水褪色,但在一定条件下,能与Cl2发生取代反应,其一氯代物只有一种,则A的结构简式为。
④若烃A能使溴水褪色,在催化剂作用下与H2加成,其加成产物分子中含有3个甲基,则A可能的结构简式为;
其中有一种分子中,所有碳原子都在同一平面内,它发生加聚反应的化学方程式为。
(2).在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、⑤C2H6;⑥CH3CH=CH2中,
一定互为同系物的是,
一定互为同分异构体的是。(填编号)
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为、;
(2)XZ2与YZ2分子的杂化轨道分别是、,立体结构分别是、,相同条件下两者在水中的溶解度较大的是(写分子式),理由是;
(3)Q的元素符号是,它属于第周期,它的核外电子排布式为,在形成化合物时它的最高化合价为;
(4)用氢键表示式 写出E的氢化物溶液中存在的所有氢键_______________________。
下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:
| a |
|||||||||||||||||
| f |
h |
i |
|||||||||||||||
| b |
e |
j |
|||||||||||||||
| c |
d |
g |
k |
||||||||||||||
| l |
(1)请写出d在元素周期表中的位置;
(2)请写出上述元素k的核外电子排布式;
(3)b、e、j三种元素的电负性由大到小的顺序(写元素符号);此三种元素的第一电离能由大到小的顺序(写元素符号);
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出e元素最高价氧化物对应的水化物与a、c、h三种元素形成的化合物反应的离子方程式;
(5)j、k、l三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素单质的性质。请写出k、l的互化物的电子式,它是由键形成的化合物(填“离子”或“共价”)。