下列命名正确的是
| A.3,3-二甲基-4-乙基戊烷 | B.3,3,4-三甲基己烷 |
| C.1,3-二甲基-4-乙基己烷 | D.2,3-二乙基-4-甲基己烷 |
25℃时将水不断滴入0.1mol/L的氨水中,下列变化的图象合理的是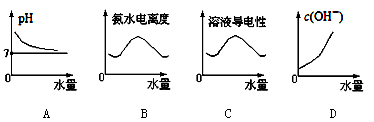
容积固定的密闭容器中存在如下反应:A(g)+3B(g) 2C(g) △H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
2C(g) △H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断一定错误的是
①图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
②图Ⅱ研究的是压强对反应的影响,且甲的压强较高
③图Ⅱ研究的是温度对反应的影响,且甲的温度较高
④图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
| A.①② | B.①③ | C.②④ | D.③④ |
某同学按照课本实验要求,用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的NaOH 溶液在右图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算中和热。下列说法中,正确的是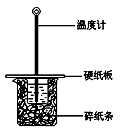
| A.实验过程中没有热量损失 |
| B.图中实验装置缺少环形玻璃搅拌棒 |
| C.烧杯间填满碎纸条的作用是固定小烧杯 |
| D.若将盐酸体积改为60 mL,理论上所求中和热不相等 |
将固体A置于密闭容器中,在一定温度下发生下列反应:
①A(s)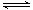 B(g)+C(g);②2C(g)
B(g)+C(g);②2C(g)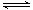 D(g)+E(g)。
D(g)+E(g)。
达到平衡时,c(D)=0.5mol·L-1,c(C)=4mol·L-1,则此温度下反应①的平衡常数为
A.25 B.20 C.16 D.9
下图表示反应N2(g)+3H2(g) 2NH3(g)ΔH=-92.2kJ/mol。在某段时间t0~t6中反应速率与反应过程的曲线图如下,则氨的百分含量最高的一段时间是
2NH3(g)ΔH=-92.2kJ/mol。在某段时间t0~t6中反应速率与反应过程的曲线图如下,则氨的百分含量最高的一段时间是
| A.t0~t1 | B.t2~t3 | C.t3~t4 | D.t5~t6 |