下图是一个乙醇燃料电池常温工作原理示意图,乙池中的两个电极一个
是石墨电极,一个是铁电极。工作时M、N两个电极的质量都不减少,则下列说法正确的是
| A.M电极的材料是石墨 |
| B.若乙池中某一电极质量增加4.32g时,理论上消耗氧气为448ml |
| C.在此过程中,甲池中OH-向通乙醇的一极移动 |
| D.在此过程中,乙池溶液中电子从M电极向N电极移动 |
下列关于有机物的说法正确的是
| A.甲烷、乙烯和苯都能与溴水反应 |
| B.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
| C.蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |
| D.苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
W |
| 原子半径/pm |
160 |
143 |
70 |
66 |
| 主要化合价 |
+2 |
+3 |
+5、+3、-3 |
-2 |
下列叙述正确的是
| A.X、Y元素的金属性:X<Y |
| B.Y的最高价氧化物对应的水化物能溶于稀氨水 |
| C.一定条件下,Z单质与W的常见单质可直接生成ZW2 |
| D.一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
设  为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
| A. | 1mol羟基中电子数为10  |
| B. | 常温常压下,22.4L乙烯中  键数为4 键数为4  |
| C. | 在反应中,每生成3mol  转移的电子数为6 转移的电子数为6  |
| D. | 常温下,1L0.1 mol·L -1的  溶液中氮原子数为0.2 溶液中氮原子数为0.2  |
能实现下列物质间直接转化的元素是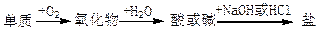
| A.硫 | B.硅 | C.铜 | D.铁 |
把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图A所示。下列说法中不正确的是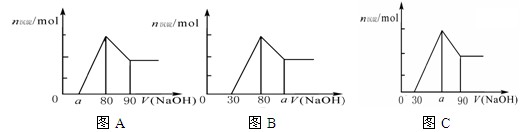
A.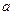 的取值范围为0≤a<50 的取值范围为0≤a<50 |
B.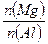 的最大值为2.5 的最大值为2.5 |
C.若将关系图改为B图时,则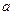 的取值范围为80<a<90 的取值范围为80<a<90 |
D.若将关系图改为C图时,则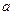 的取值范围为75<a<90 的取值范围为75<a<90 |