物质A~E都是由下表中离子组成的,常温下各物质从1mL稀释到1000mL,pH的变化如图甲所示,其中A与D反应得到E。 请回答:
| 阳离子 |
NH4+、H+、Na+ |
| 阴离子 |
OH-、CH3COO-、Cl- |

(1)根据pH的变化关系图甲,写出物质的化学式:B: ,D: 。
(2)图甲a>9的理由是
(3)另取浓度为C1的B溶液25mL,向其中逐滴滴加0.2mol/L的D溶液,滴定过程中溶液pH的变化曲线如乙图所示。
①C1为 ;
②G点溶液呈中性则滴加入D溶液的体积V 12.5mL(填>,<或=)
③常温下B、C溶液的pH分别是a、b且a+b=13则将B、C混和恰好完全 反应时所消耗B、C溶液的体积比VB:VC=
反应时所消耗B、C溶液的体积比VB:VC=
开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的。
Ⅰ.由C、H、O三种元素中的两种和三种分别组成的燃料物质甲和乙,其分子中均有氧,且1个乙分子中含有18个电子,则甲和乙分别是________。乙是一种清洁燃料,工业上可用甲和氢气反应制得。
(1)T1温度时,在体积为2 L的密闭容器中充入2 mol甲和6 mol H2,反应达到平衡后,测得c(甲)=0.2 mol/L,则乙在平衡混合物中的物质的量分数是。
(2)升高温度到T2时,反应的平衡常数为1,下列措施可以提高甲的转化率的是________(填字母)。
A.加入2 mol甲B.充入氮气
C.分离出乙D.升高温度
Ⅱ.(1)甲烷也是一种清洁燃料,但不完全燃烧时热效率降低并会产生有毒气体造成污染。
已知:①CH4(g) + 2O2(g) = CO2(g) + 2H2O(l)ΔH1=―890.3 kJ/mol
②2CO (g) + O2(g) = 2CO2(g) ΔH2=―566.0 kJ/mol
则甲烷不完全燃烧生成一氧化碳和液态水时的热效率只是完全燃烧时的________倍(计算结果保留1位小数)。
(2)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol/L的氯化铜溶液的装置示意图:
请回答:
①若使用酸性水溶液做电解质,甲烷燃料电池的负极反应式是________。
若使用熔融Na2CO3做电解质,该电池负极的反应式是。
若使用燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,可以传导O2—。则在电池内部O2—由____极移向____极(填“正”或“负”);电池的负极电极反应式为。
②若B中为氯化铜溶液,当线路中有0.1 mol电子通过时,________(填“a”或“b”)极增重________g。
若B中为足量Mg(NO3) 2和NaCl的混合溶液。电解开始后阴极的现象为____。
海水的综合利用,现有流程图如下:
Ⅰ工业上以粗食盐(含有少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3。请回答:
(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有。
(2)将CaO投入含有大量的NH4Cl的母液中,能生成可循环使用的NH3,该反应的化学方程式是。
(3)向饱和食盐水中首先通入的气体是,过程Ⅲ中生成NaHCO3晶体的反应的化学方程式是。
(4)碳酸钠晶体失水的能量变化示意图如下:
Na2CO3·H2O (s) 脱水反应的热化学方程式是。
(5)产品纯碱中常含有NaCl。取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体。则该产品中Na2CO3的质量分数是。
Ⅱ电解饱和食盐水所得气体X,可应用于提取溴单质。请回答:
(1)气体X的化学式为,反应II的化学方程式为。
(2)在母液苦卤中含有较多的NaCl、KCl、MgCl2、MgSO4等物质。用沉淀法测定苦卤中镁元素的含量(g/L),实验过程中应测定的数据有。
(3)电解200kg 质量分数为25%的饱和食盐水,当浓度下降到20%时,收集到氯气的物质的量为(溶于溶液中的氯气忽略不计,计算结果保留一位小数) 。
(12)下图中的每一方框内表示一种反应物或生成物,其中A、C、D、E、F在通常情况下均为气体,且A与C物质的量之比为1:1。B为常见液体。
试回答下列问题:
(1)X是;F是(都填化学式)。
(2)A D反应的化学方程式。
D反应的化学方程式。
(3)G与Cu的反应中,G表现得性质有。
(4)X与过量NaOH溶液反应(加热)的离子方程式。
(5)以C、B、D为原料可生产G,若使a mol C 完全转化为G,理论上至少需要Dmol。
(1)下列有关实验操作或判断不正确的是。
| A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏小 |
| B.用干燥的pH试纸测定氯水的pH |
| C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 |
| D.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量 |
E.观察钾元素焰色反应的操作:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,观察.
F.制备氢氧化亚铁时,将盛有NaOH溶液的滴管,伸入硫酸亚铁溶液中
(2)除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处。
| 试剂 |
离子反应方程式 |
|
| ①NaHCO3溶液(Na2CO3) |
||
| ② Fe2O3(Al2O3) |
||
| ③FeCl3溶液(FeCl2) |
||
| ④CO2(HCl) |
某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题: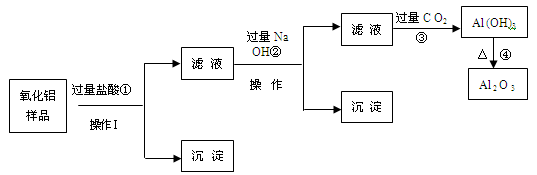
(1)沉淀A的成分是(填化学式),沉淀B的成分是(填化学式);
(2)滤液A中若加入过量的铁粉,可能发生的所有离子方程式为、;
(3)在操作Ⅰ的名称是,其中玻璃棒的作用是。