A、B、C、D和甲有以下转化关系。已知物质甲是短周期元素组成的盐,且是某 种消毒液的有效成分,沉淀D可溶于酸。
种消毒液的有效成分,沉淀D可溶于酸。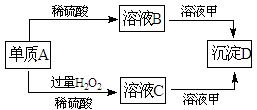
请回答下列问题:
(1)组成A的元素在周期表中位于第 周期第 族。
(2)鉴定C中阳离子(不考虑H+)的操作和现象是 。
(3)A转化为B时会放出无色气体E,在298K时1mol A完全反应放出热量QkJ,则该反应的热化学方程式为 。
(4)若A转化为C时无气体放出,写出该反应的化学方程式:
。
(5)写出溶液 C和溶液甲反应的离子方程式: 。
C和溶液甲反应的离子方程式: 。
选择恰当的试剂和方法除去下列物质中的少量杂质(括号内为杂质)
(1)C2H6(C2H4)试剂__________,方法:_____________________________________。
(2)溴苯(溴)试剂__________,方法:________________________________________。
(3)苯(甲苯)试剂_______,方法:_______________________________________。
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题: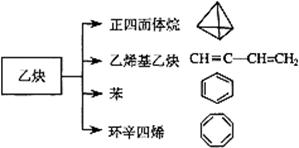
(1)正四面体烷的分子式为;二氯苯的结构有种。
(2)关于乙烯基乙炔分子的说法错误的是
| A.1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应 |
| B.乙烯基乙炔分子内含有两种官能团 |
| C.等质量的乙烯基乙炔与正四面体烷完全燃烧时的耗氧量不相同 |
| D.乙烯基乙炔既是乙烯的同系物又是乙炔的同系物 |
(3)写出与环辛四烯互为同分异构体且属于芳香族化合物的分子的结构简式:
(4)写出与苯互为同系物且苯环一氯代物只有两种的物质的结构简式(举两例):
________________________、________________________
已知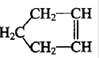 可简写为
可简写为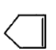
降冰片烯的分子结构可表示为: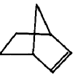
(1)降冰片烯属于__________。
a.环烷烃 b.不饱和烃 c.烷烃 d.芳香烃
(2)降冰片烯的分子式为__________。
(3)降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为____。
(4)降冰片烯不具有的性质__________。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(6分)下列各组中的两种有机物,可能是相同的物质.同系物或同分异构体等,请判断它们之间的关系
(1)2-甲基丁烷和丁烷 ________________
(2)新戊烷和2,2-二甲基丙烷_____________
(3)1,3-二甲基苯和乙苯 __________________
(4分)写出相对分子质量为128的烃的分子式:________、________。