(1)稀释0.1 mol·L-1氨水时,随着水量的增加而减小的是 (填写序号)。
① ②
②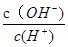 ③c(H+)和c(OH-)的乘积 ④OH-的物质的量
③c(H+)和c(OH-)的乘积 ④OH-的物质的量
(2)pH相同的等体积的A、B两份溶液(A为盐酸,B为醋酸)分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是________(填写序号)。
①反应所需的时间B>A ②开始反应时的速率A>B
③参加反应的锌粉物质的量A=B ④反应过程中的平均速率B>A
⑤A溶液里有锌粉剩余 ⑥B溶液里有锌粉剩余
(3)将等体积、等物质的量浓度的氨水和盐酸混合后,升高温度(溶质不会分解)溶液的pH随温度变化是图中的_________曲线(填写序号) 。

(4)室温下,向0.1mol·L-1的盐酸与0.2mol·L-1 的氨水等体积混合,则所得溶液中所有离子物质的量浓度由大到小的顺序为______________ 。
(5)由电离常数可知酸性强弱:CH3COOH>H2CO3>HCO3-,则浓度相同的下列溶液碱性由强到弱顺序为: (填序号)
①CH3COONa ②NaHCO3 ③Na2CO3
(6)氯化铁溶液呈酸性的原因是(用离子方程式表示): 。
某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B=H++HB-;HB- H++B2-
H++B2-
完成下列问题:在0.1 mol/L 的Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol/L B.c(Na+)+c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-) D.2c(Na+)=c(B2-)+c(HB-)
下图中各方框中的字母表示有关的一种反应物或生成物(某些物质略去)其中常温下B、D、G、I、J为气体,其中B可使湿润的红色石蕊试纸变蓝,A~N的所有物质中只有G为单质,其余为化合物。N为不溶于水的无机酸。
请回答下列问题:
(1) 写出下列物质的化学式
A:_______________F:____________L:________________
(2) 写出G的一种同素异形体的化学式:
(3)已知工业上生产0.1molB放出4.62kj热量,写出该反应的热化学方程式:
(4)在反应C+E→G +F中,每生成1molG转移 mol电子。
+F中,每生成1molG转移 mol电子。
在一容积为2 L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,反应中NH3的物质的量浓度的变化情况如下图:
2NH3(g) ΔH<0,反应中NH3的物质的量浓度的变化情况如下图:

请回答下列问题:
(1)该反应的化学平衡常数K表达式为______________________;
升高温度K值(填“变大”、“变小”或“不变”)
(2)根据上图,计算从反应开始到平衡时,平均反应速率v(H2)为____________。
(3)判断该反应 达到平衡状态的标志是(填字母);
达到平衡状态的标志是(填字母);
a.N2和NH3浓度相等b.NH3百分含量保持不变
c.容器中气体的压强不变 d.NH3的生成速率与H2的消耗速率相等
e.容器中混合气体的密度保持不变
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为_______________。
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d.0.08 mol/L
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L),请在上图中画出第5分钟末达到此平衡时NH3浓度的变化曲线。
(1)某厂废水中含KCN,其浓度为650mg·L-1现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2=KOCN+2KCl+H2O被氧化的元 素是_________。
素是_________。
(2)若将等浓度等体积的KCN与HCN混合,测得溶液中c(K+)>c(CN-),则该溶液的pH______7,要使c(K+)=c(CN-),应采取的措施是____________________________.。
(3)若将10m3含KCN的浓度为650mg·L-1的废水中KCN氧化除去,需要标准状况下的氯气的体积为____________L。
(4)已知:
 则
则 的△H是_________________。
的△H是_________________。
(8分)A、B、C、D、E、F均为短周期元素,其原子序数依次增大。已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;D是地壳中含量最高的元素;D和F、A和E分别同主族;E是所有短周期主族元素中原子半径最大的元素。根据以上信息回答下列问题:
(1)B与D形成化合物BD2的结构式为。 (2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式。 FB2气体通入BaCl2和甲的混合溶液,生成白色沉淀和无色气体CD,有关反应的离子方程式为__________________________。
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式。 FB2气体通入BaCl2和甲的混合溶液,生成白色沉淀和无色气体CD,有关反应的离子方程式为__________________________。
(3)均由A、D、E、F四种元素组成的两种盐,其相对 分子质量相差16,写出它们在溶液中相互作用的离子方程式为______
分子质量相差16,写出它们在溶液中相互作用的离子方程式为______ _________________________
_________________________ ___________;由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)____________________________________________________________________。
___________;由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)____________________________________________________________________。
(4)C2A4 ─ 空气燃料电池是一种碱性燃料电池。电解质溶液是20%~30%的KOH溶液。则燃料电池放电时,负极的电极反应式为__________________________________.。
在80℃时,将0.40 mol的N2O4气体充入1 L固定容积的密闭容器中发生反应:N2O4  2NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:
2NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:
| 时间(s) |
0 |
20 |
40 |
60 |
80 |
100 |
| n(N2O4)(mol) |
0.40 |
a |
0.20 |
c |
d |
e |
| n(NO2)(mol) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)在20s — 40s之间,用N2O4表示的平均反应速率为。
(2)在80℃时该反应的平衡常数K=。
(3)要增大该反应的平衡常数,可采取的措施有(填序号)。
①增大N2O4的起始浓度②向混合气体中通入NO2
③使用高效催化剂④升高温度
(4)反应进行至100s后若降低温度,混合气体的颜色(填“变浅”、“变深”或“不变”)。
(5)反应进行至100s后若向容器中再充入0.40 mol的N2O4气体,则达到新平 衡后N2O4的转化率将(填“增大”、“减小”或“不变”)。
衡后N2O4的转化率将(填“增大”、“减小”或“不变”)。