亚硫酸钠是食品加工中广泛使用的漂白剂、防腐剂和抗氧化剂,其在食品中的残留量通常以二氧化硫含量计算。
(1)亚硫酸盐具有一定的毒性,长期摄入过量的亚硫酸盐,红细胞和血红蛋白会减少,钙的吸收也会减少,原因是 。
检验某黑木耳中是否含有亚硫酸盐的简单方法是:将黑木耳样品剪成碎末放入烧杯,加入20mL水和10mL盐酸,加热一会儿,滴入试剂A,观察现象既可。
(2)加热的作用是 ,加热时间不能太长的原因是 。
(3)试剂A是 。
在足量的亚硫酸钠溶液中加入1~2滴液溴,振荡后溶液变为无色。
(4)写出以上反应的离子方程式 。
(5)以上反应后的溶液中含有SO32-、HSO3-、SO42-、Br-、OH-等阴离子。设计实验检验SO42- 和Br-,写出实验方法。试剂不限。
| 实验操作 |
预期现象与结论 |
| 步骤1: |
|
| 步骤2: |
|
(1) “笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为N2O与CO2分子具有相似的结构(包括电子式);又已知N2O分子中氧原子只与一个氮原子相连,则N2O的电子式可表示为,它(填“含有”或“不含”)非极性键。
(2)有以下物质:①CH4,②Cl2,③H2O,④N2,⑤C2H4,⑥C2H6,⑦H2,⑧Na2O2,⑨HCN(H—C≡N);只含有极性键且为非极性分子是__________;含有非极性键的共价化合物是__________;既有σ键又有π键的化合物是__________;
现有甲、乙、丙、丁四种晶胞(如图所示),可推知:甲晶体中A与B的离子个数比为;乙晶体的化学式为;丙晶体的化学式为______;丁晶体的化学式为______。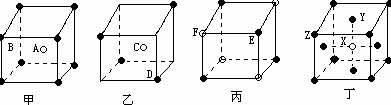
m mL三种气态烃混合物与足量氧气混合点燃后,恢复到原来状况(常温、常压)气体体积共缩小2m mL,这三种烃可能的组合是________ 、_____________、 ______________(写三组)
(1)分别写出相对分子质量为128、72的烃的分子式:______、_ ___、__ ___(可不写满,也可补充)
(2)立方烷的结构简式如图所示,每个顶点是一个碳原子。则: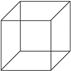
①其分子式为_____________。②它的一氯取代物有_____________种。③它的二氯取代物有_____________种。
A是分子式为C7H8的芳香烃,已知它存在以下一系列转化关系,其中C是一种一元醇,D是A的对位一取代物,H与E、I与F分别互为同分异构体。
(1)化合物I的结构简式是__________________,反应B→C的化学方程式是__________________;
(2)设计实验证明H中含有溴原子,还需用到的试剂有___________________________;
(3)为验证E→F的反应类型与E→G不同,下列实验方法切实可行的是_________________。
| A.向E→F反应后的混合液中加入硝酸酸化,再加入AgNO3溶液得到淡黄色沉淀 |
| B.向E→F反应后的混合液中加入溴水,发现溴水立即褪色 |
| C.向E→F反应后的混合液中加入盐酸酸化后,加入溴的CCl4溶液,溶液褪色 |
| D.向E→F反应后的混合液中加入酸性KMnO4溶液,混合液红色变浅 |