叠氮化合物应用广泛,如NaN3,可用于汽车安全气囊,PhCH2N3可用于合成化合物V(见下图,仅列出部分反应条件Ph—代表 苯基)
苯基)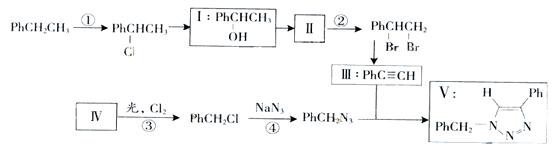
(1)下列说法不正确的是 (填字母,1分)
A. 反应①、④属于取代反应
B. 化合物I可发生消去反应,但不能发生氧化反应
C. 一定条件下化合物Ⅱ能生成化合物I
D. 一定条件下化合物Ⅱ能与氢气反应,反应类型与反应②相同
(2) 化合物Ⅱ发生聚合反应的化学方程式为(不要求写出反应条件)
(2分)
(3)化合物Ⅲ与PhCH2N3发生环加成反应成化合物V,不同条件下环加成反应还可生成化合物
V的同分异构体。该异构体的结构式为 。(2分)
(4) 科学家曾预言可合成C(N3)4,其可分解成单质,用作炸药。有人通过NaN3与N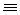 C-CCl3,反应成功合成了该物质。下列说法正确的是 (填字母,2分.)。
C-CCl3,反应成功合成了该物质。下列说法正确的是 (填字母,2分.)。
A. 该合成反应可能是取代反应
B. C (N3)4与
(N3)4与 甲烷具有类似的空间结构
甲烷具有类似的空间结构
C. C(N 3)4不可能与化合物Ⅲ发生环加成反应
3)4不可能与化合物Ⅲ发生环加成反应
D. C(N3)4分解爆炸的化学反应方程式可能为:C(N3)4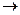 C+6N2↑
C+6N2↑
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一。其中炉渣的主要成分 是FeO、Fe2O3、SiO2、Al2O3。各物质有如下转化关系,请回答:
(1)写出能证明SO2具有氧化性且现象明显的化学方程式________________。
(2)用NaOH溶液吸收SO2所得NaHSO3溶液pH<7,则该溶液中存在离子的物质的量浓度由大到小的顺序是________。
(3)写出Cu2S熔炼制取粗铜的化学方程式________________________
(4)废电解液中常含有Pb2+、Zn2+,向废电解液中加入Na2S溶液,当有PbS和ZnS沉淀时,C(Zn2+): C(Pb2+)=________。[已知:Ksp(PbS)=3.4×10-28mol2·L-2、Ksp(ZnS)=1.6×10-24mol2·L-2)]
(5)写出证明溶液I中含有Fe2+的实验过程________________。
(6)Na2FeO4能杀菌净水的原因是________________。
(7)Na2FeO4和Zn可以组成碱性电池,其反应式为:3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)+4OH-。请写出放电时正极电极反应式________________。
研究硫及其化合物对于工农业生产具有重要意义。
(1)图Ⅰ所示一个容积为4L的密闭容器,内有可移动的隔板。一定温度(T)下,左室加入2 mol SO3,右室加入2 mol SO2和1 mol O2,在少量催化剂存在下分别发生反应:
左室:
右室:
反应达到平衡时,右室反应过程和能量关系如图Ⅱ所示。
①ΔH2=_______(含a的数学式表示);反应的平衡常数K=_________L·mol-1。
②能说明两边反应一定达到平衡的是______________(填序号)。
A.隔板不再移动
B.左右两边SO2的物质的量相等
C.左右二室中SO2与O2物质的量之比都是2∶1
③达平衡时,左室反应吸收的热量为Q1kJ,右室反应吸收的热量为Q2kJ,则Q1、Q2满足的关系是_____________(填序号)。
A.Q1=Q2
B.Q1>Q2
C.Q1<Q2
(2)高温下,炽热的Cu2S与水蒸气反应生成金属铜、H2和SO2( )。
)。
①写出该反应的化学反应方程式_____________________________________________。
②若有1 mol Cu2S参与反应,则转移电子的物质的量是_________mol。
已知:下列反应是有机合成的重要成环反应。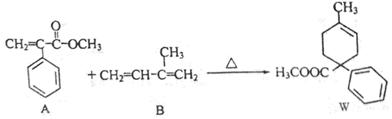
化合物A可由化合物C合成,其流程为:
(1)A+B→W的反应类型是______________,物质H的名称是_________________。
(2)由C得到D需要经过两步反应,其反应过程中需要的试剂依次是___________。
(3)写出D→E的化学方程式______________________________________________。
(4)物质X是G的同分异构体,请写出符合下列条件的X的结构简式________________。(任写一种)
①苯环上有三个取代基 ②1 mol X与足量银氨溶液反应能生成4 molAg
铜及其合金是人类最早使用的金属材料。
(1)写出铜原子价电子层的电子排布式____________;与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有_______________(填元素符号)。
(2)波尔多液是一种保护性杀菌剂。胆矾晶体是配制波尔多液的主要原料,其结构示意图可简单表示如右图:
①胆矾的化学式用配合物的形式表示为_______。
②胆矾中含有的作用力除极性共价键、配位键外还有__________。
③胆矾晶体中杂化轨道类型是sp3的原子是_____________。
(3)赤铜矿的晶胞结构如图所示,铜原子的配位数为_________。
科研、生产中常涉及钠、硫及其化合物。
(1)工业上用Na2CO3溶液处理水垢中的CaSO4,反应的离子方程式为___________________;实验室中,Na2S溶液长期放置有硫析出,原因为___________________(用离子方程式表示)。
(2)下图是大型蓄电系统的示意图。左右两侧为电解质储罐,中央为电池,反应原理为: ,电解质通过泵在储罐和电池间循环;离子选择性膜只允许钠离子通过。
,电解质通过泵在储罐和电池间循环;离子选择性膜只允许钠离子通过。
当蓄电池放电时,电池中Na+的移动方向是_________(填“a→b”或“b→a”),电极a的电极反应式为_______________;当蓄电池处于充电状态时,电极b的电极反应式为___________。用该电池做电源,采用惰性电极电解200 mL 1 mol·L-1的AgNO3溶液,当阴极质量增加2.16 g时,电解后溶液的pH为_________(不考虑溶液体积变化)。
(3)工业上,用Na2SO3溶液作为吸收液可吸收烟气中的SO2,吸收SO2过程中,溶液pH与 关系如下表:
关系如下表:
 |
91∶9 |
1∶1 |
9∶91 |
| pH(25℃) |
8.2 |
7.2 |
6.2 |
①由上表判断,NaHSO3溶液显________性,用平衡原理解释:__________________。
②当溶液呈中性时,溶液中离子浓度的大小关系为_____________________________。