[化学——选修物质结构与性质]
乙炔是有机合成工业的一种原料。工业上曾用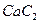 与水反应生成乙炔。
与水反应生成乙炔。
(1)将乙炔通入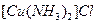 溶液生成
溶液生成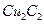 红棕色沉淀。
红棕色沉淀。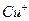 基态核外电子排布式为 。
基态核外电子排布式为 。
(2) Ca2+的原子结构示意图: ;已知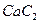 中
中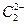 与
与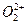 互为等电子体,
互为等电子体,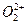 的电子式可表示为 ;1mol
的电子式可表示为 ;1mol 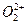 中含有的
中含有的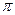 键数目为 。
键数目为 。
(3)乙炔与氢氰酸反应可得丙烯腈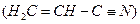 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
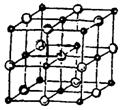
(4)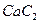 晶体的晶胞结构与
晶体的晶胞结构与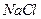 晶体的相似(如下图所示),但
晶体的相似(如下图所示),但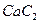 晶体中含有的哑铃形
晶体中含有的哑铃形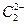 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。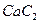 晶体中1个
晶体中1个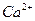 周围距离最近的
周围距离最近的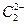 数目为
数目为  。
。
以下列出了四种物质的分子结构示意图。其中圆圈表示原子核(包含除价电子以外的电子)的示意图,黑点表示非共用电子对,直线表示共价键,且图中各分子仅是由第一、二周期元素的原子构成的。在括号内填写四种物质的分子式。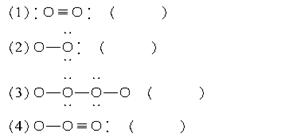
a、b、c、d、e是短周期元素,周期表中a与b、b与c相邻;a与e的最外层电子数之比为2∶3,b的最外层电子数比e的最外层电子数少1;常见化合物d2c2与水反应生成c的单质,且溶液使酚酞试液变红。
(1)e的元素符号是________。
(2)a、b、c的氢化物稳定性顺序为(用分子式表示)________________________;b的氢化物和b的最高价氧化物对应的水化物反应生成Z,则Z的化学式为________,d、e形成化合物的电子式为________________。
(3)一定量的d2c2与ac2反应后的固体物质,恰好与0.8 mol稀盐酸完全反应,并收集到0.25 mol气体,则用物质的量表示该固体物质的组成为________________。
有A、B、C三种元素,已知①4 g A元素的单质与水作用,在标准状况下放出氢气2.24 L,反应中有1.204×1023个电子发生转移;②B元素可与A元素形成AB2型的离子化合物,且知A、B的离子具有相同的核外电子排布;③元素C的气态氢化物可以与其最高价氧化物对应的水化物发生非氧化还原反应生成盐,1 mol该盐含有42 mol电子。
根据以上信息填写下列空白:
(1)元素符号:A:________,B:________,C:________。
(2)A元素的离子结构示意图为__________________________________________。
(3)用电子式表示AB2的形成过程__________________________________
________________________________________________________________________。
(4)C的气态氢化物与B的气态氢化物反应时有________________现象发生,生成物的化学式为________,它属于________化合物。
A+和B2-都与Ar具有相同的电子层结构,则A的元素符号为________,B元素的原子结构示意图为____________,它们形成的化合物的电子式为________________,A+和B2-离子半径大小比较为________________。
(12分)化合物A由周期不同的短周期元素X、Y组成,是良好的耐热冲击材料。
(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X的原子结构示意图为________。
(2)X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为________________________。
(3)一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子。
①Z与H2O2反应,其产物之一是Y的单质,Y的单质的电子式为________;Z分子的结构呈________。
②A的化学式是________。
(4)X的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是______________________________________________。