Ⅰ.某探究小组用HNO3与大理石反应过程中固体质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K。请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 |
T/K |
大理石 质量/g |
规格 |
HNO3浓度/mol·L-1 |
HNO3 体积/ mL |
实验目的 |
| ① |
298 |
10.00 |
粗 |
1.00 |
25.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响。 |
Ⅱ.某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理,并说明理由 。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;3mol/L H2SO4、3%H2O2、6mol/L HNO3、0.01mol/L KMnO4、NaOH稀溶液、0.1mol/L KI、20%KSCN、蒸馏水。
① 提出合理假设
假设1: ;
假设2: ;
假设3: 。
② 基于上述假设,设计实验方案。请在答题卡上按下表格式写出实验操作步骤、预期现象与结论。
| 实验操作 |
预期现象与结论 |
| 步骤1 |
|
| 步骤2 |
|
| 步骤3 |
|
| …… |
|
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答: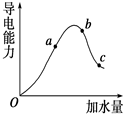
(1) “O”点为什么不导电________.
(2)a,b,c三点的pH由小到大的顺序是____________.
(3) a、b、c三点中电离程度最大的是
电离平衡常数Ka、Kb、Kc的大小关系为________.
(4)若使c点溶液中的c(CH3COO-)增大,可以采取下列措施中的 ________(填序号).
A加热;B加很稀的NaOH溶液;C加NaOH固体;D加水;E加固体CH3COONa;F加入锌粒
研究NO2、、CO等大气污染气体的处理具有重要意义。
利用反应6NO2(g)+8NH3(g)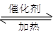 7N2(g)+12 H2O(g)可处理NO2。700℃时,向容积为2L的密闭容器中充入一定量的NO2和NH3, 反应过程中测定的部分数据见下表
7N2(g)+12 H2O(g)可处理NO2。700℃时,向容积为2L的密闭容器中充入一定量的NO2和NH3, 反应过程中测定的部分数据见下表
| 反应时间/min |
n(NO2)/mol |
n(NH3)/ mol |
| 0 |
1.20 |
1.60 |
| 2 |
0.90 |
|
| 4 |
0.40 |
(1)反应在2min内的平均速率为v(NH3)=
4min该反应达到平衡状态,则该反应的平衡常数K的表达式为,NO2的转化率为
(2) 700℃ ,将NO2与NH3以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
a.体系压强保持不变 b.混合气体颜色保持不变
c.体系密度保持不变 d.每消耗1 mol NO2的同时生成2 mol H2O
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。200℃时,向在一个带活塞的密闭真空容器中中充入一定量的CO和H2发生上述反应,压缩容器的容积为原来的一半,平衡将移动(填向左,向右,不);CO的浓度将(增大,减小,不变)
CH3OH(g)。200℃时,向在一个带活塞的密闭真空容器中中充入一定量的CO和H2发生上述反应,压缩容器的容积为原来的一半,平衡将移动(填向左,向右,不);CO的浓度将(增大,减小,不变)
2SO2(g)+O2(g) 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。
2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。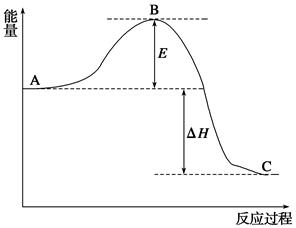
请回答下列问题:
(1)图中A、C分别表示__________、__________,E的大小对该反应的反应热有无影响?____________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?___________。
(2)图中ΔH=__________kJ/mol;
(3)如果反应速率v(SO2)为0.05 mol/(L·min),则v(O2)=____mol/(L·min)
(4)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH=_。
把煤作为燃料可通过下列两种途径:
途径I:C(s) +O2 (g)=CO2(g)△H1<0①
途径II:先制成水煤气:C(s) +H2O(g)=CO(g)+H2(g)△H2>0②
再燃烧水煤气:2CO(g)+O2 (g)=2CO2(g)△H3<0③
2H2(g)+O2 (g)=2H2O(g)△H4<0④
请回答下列问题:
(1)途径I放出的热量( 填“大于”“等于”或“小于”) 途径II放出的热量。
(2)△H1、△H2、△H3、△H4的数学关系式是。
(3)12g炭粉在氧气中不完全燃烧生成一氧化碳,放出110.35kJ热量。其热化学方程式为。
(4)煤炭作为燃料采用途径II的优点有。
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据
回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为__________mol·L-1。
(2)在容量瓶的使用方法中,下列操作不正确的是____________(不定项选择)
| A.使用容量瓶前检验是否漏水 |
| B.容量瓶用水洗净后,再用待配溶液洗涤 |
| C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。 |
| D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。 |
(3)甲、乙两同学欲用上述浓盐酸和蒸馏水配制250 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
①每位同学各需要量取________mL上述浓盐酸进行配制。(保留小数点后一位)
②在配制过程中,甲同学存在以下不正确操作,对所配制的稀盐酸的物质的量浓度有何影响?(在横线上填“偏大”、“偏小”或“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
③乙同学转移溶液时操作如图所示,其中存在的错误是____________________________________________。