某温度下,水的离子积为Kw,该温度下将a mol·L-1的一元酸HA与b mol/L的一元碱BOH等体积混合,若混合液显中性,必须满足的条件是
| A.a=b | B.c(H+)=c(OH-)=10-7mol·L-1 |
| C.混合液中Kw=c2(OH-) | D.c(H+)+c(B+)=c(OH-)+c(A-) |
已知A、B、C、X是四种中学化学中常见的物质,其转化关系符合下图。则A和X(要求A和X能互换)不可能是
A.C和O2
B.SO2和NaOH溶液
C.Cl2和Fe
D.AlCl3溶液和NaOH溶液
下列根据实验操作和现象所得出的结论正确的是()
| 选项 |
实验操作 |
实验现象 |
结 论 |
| A |
用铂丝蘸取溶液进行焰色反应 |
火焰呈黄色 |
溶液中无K+ |
| B |
向溶液中先滴加稀盐酸,再滴加BaCl2溶液 |
先滴加稀盐酸无现象,滴加BaCl2后出现白色沉淀 |
溶液中一定含有SO42- |
| C |
向某溶液中加入稀盐酸 |
产生使澄清石灰水变浑浊的气体 |
溶液中一定含有CO32- |
| D |
向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 |
试纸不变蓝 |
原溶液中无NH4+ |
利用下列各组物质制备和收集少量相应气体,能采用如图实验装置的是 ( )
①浓氨水与固体CaO ②稀盐酸与石灰石
③稀硝酸与铜片④过氧化氢溶液与MnO2
⑤锌粒与稀硫酸⑥浓盐酸与MnO2
| A.①②⑥ | B.②④ | C.①②③⑥ | D.全部 |
下列观点正确的是 ( )
| A.化合物电离时,生成的阴离子是氢氧根离子的是碱 |
| B.某化合物的熔融状态能导电,该化合物中一定有离子键 |
| C.某化合物的水溶液能导电,该化合物一定是电解质 |
| D.某纯净物在常温下为气体,则组成该物质的微粒一定含有共价键 |
下图所示的实验,能达到实验目的的是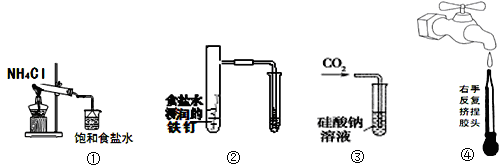
| A.实验①制取的氨气溶解在饱和NaCl溶液 |
| B.实验②通过观察右边试管有无倒吸现象说明铁钉是否发生吸氧腐蚀 |
| C.实验③可用于证明碳的非金属性比硅强 |
| D.图④是实验室洗涤胶头滴管的操作 |