化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
。
(2)现有一瓶胃舒平药片(复方氢氧化铝),请设计实验验证其主要成分。(写出实验步骤和实验现象):
将药片碾碎,
则说明其主要成分为氢氧化铝。
(3)自选合适的氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应方程式:__________________________________________ ______。
检验Fe3+常用的试剂除碱外,还可以用 (填化学式),现象是 。
空气吹出法是目前从海水中提取溴的常用方法,流程如下(苦卤:海水蒸发结晶分离出食盐后的母液):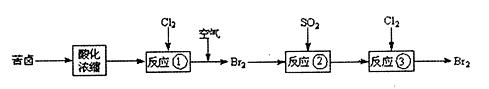
(1)反应①的离子方程式为。
(2)反应②中的还原剂是。
(3)实验室从反应③后的溶液中分离出单质溴的方法是、、蒸馏。
(4)苦卤还可以用来制取金属镁,用化学方程式或离子方程式表示从苦卤制取金属镁的反应原理
下表为元素周期表的一部分,请参照元素①—⑧在表中的位置,用化学用语回答下列问题: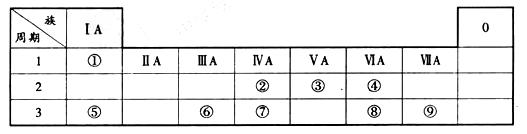
(1)④、⑤、⑥的原子半径由大到小的顺序为(填元素符号)。
(2)②、③、⑦的最高价音氧睦的酸性由强到弱的顺亭是【填化学式】。
(3)①、④,⑤、⑨中的某些元素可形成既舍离子键又含共价键的化合物.写出其中任意一种化合物的电子式:。
(4)由②和④组成,且②和④的质量比为3:8的化合物的结构式是。
(5)⑥单质与⑤的屉高价氧化物的水化物反应的离子方程式为。
(6)⑧ 、⑨两元素非金属性较强的是(写元素符号),举二个例子说明推
、⑨两元素非金属性较强的是(写元素符号),举二个例子说明推 断依据:。
断依据:。
根据要求填空:
(1)根据要求写出下列反应的化学方程式:
①有水参加的置换反应,承作氧化剂
②有水参加的氧化还原反应,水既是氧化剂又是还原剂。
③有水参加的氧化还原反应.但水既不是氧化剂又不是还原剂。
④有水参加的复分解反应。
(2)“绿色试剂”双氧水可作为矿业废渣消毒剂,消除采矿业艘液中的氰化物(如KCN)的化学方程式为:KCN+H2O2+H2O=A+NH3↑
①生成物A的化学式为。
②在标准状况下有0.448L氨气生成.则转移的电子数为。
③反应中被氧化的元素为。
(3)同温同压下,同体积的NH3和H2S的质量比是;同质量的NH3和H2S的体积比是;若两者所吉氢原于个数相等,NH3和H2S的物质的量比是。
(4)将标准状况下的NH3(g)VL溶于水中,得到密度为b g·cm-3的氨水a g,此时物质的量浓度为c mol·L-1,则溶于水中的NH3(g)的体积V是L(用a、b、c等表示)。
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图: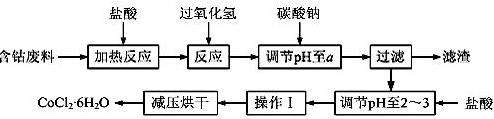
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Co(OH)2 |
Al(OH)3 |
| 开始沉淀 |
2.3 |
7.5 |
7.6 |
3.4 |
| 完全沉淀 |
4.1 |
9.7 |
9.2 |
5.2 |
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为 。
。
(2)加入碳酸钠调节pH至a,a的范围是;
(3)操作Ⅰ包含3个基本实验操作,它们是、和过滤。
(4)制得的CoCl2·6H2O需减压烘干的原因是 。
(5)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是(任写1点)。
(12分)
随着氮氧化物污染的日趋严重,国家将于“十二五”期间加大对氮氧化物排放的控制力度。目前,用活性炭还原法处理氮氧化物是消除氮氧化物污染的有效方法。
⑴已知产物 A、B 都是参与大气循环的气体,请结合下表数据写出NO与活性炭反应的化学方程式:
⑵某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol·L-1
时间/min |
NO |
A |
B |
||
| 0 |
0. 10 |
0 |
0 |
||
| 10 |
0.058 |
0.021 |
0.021 |
||
| 20 |
0.040 |
0.030 |
0.030 |
||
| 30 |
0.040 |
0.030 |
0.030 |
||
| 40 |
0.032 |
0. 034 |
0.017 |
||
| 50 |
0.032 |
0. 034 |
0.017 |
①T1℃时,求该反应平衡常数(列出K的表达式,要求计算过程)。
②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是 。
③若30min后升高温度至T2℃,达到平衡时,容器中NO、A、B的浓度之比为5:3:3,则该反应的△H 0(填“>”、“=”或“<”)。
④压缩容器体积,增大压强对该反应的反应速率和平衡移动的影响是 。