(20分)某同学用废干电池内的黑色固体(可能含有MnO2、NH4Cl、ZnCl2等物质)进行如图所示实验: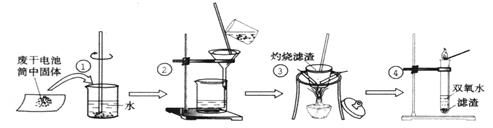
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、 、 、
等(只需答出三种仪器即可);
(2)操作④的试管加入③中所得滤渣,试管中迅速产生能使带火星的木条复燃的气体,由此推测滤渣可能为MnO2,试管中发生反应的化学方程式: ;
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的物质为: 。
(4)已知氯化锌与稀氨水反应先生成Zn(OH)2白色沉淀,Zn(O H)2可以溶于稀氨水生成可溶性的Zn(NH3)4(OH)2;下列是该同学对操作②的滤液主次成分进行探究的过程:
H)2可以溶于稀氨水生成可溶性的Zn(NH3)4(OH)2;下列是该同学对操作②的滤液主次成分进行探究的过程:
[猜想I]:主要成分为氯化铵;
[验证(操作)过程]:取少量滤液加入NaOH固体,并加热;
[实验现象]:闻到有轻微的氨味;
[判断猜想]: (填“猜想I成立”或“猜想I不成立”);
[猜想II]:主要成分为氯化锌;
[验证(操作)过程]: ;
[实验现象]: ;
[判断猜想]:猜想Ⅱ成立;由上述实验得出结论:
操作②的滤液中的主要成分为: ;次要成分为: 。
实验室需用 晶体配制
晶体配制 的
的 溶液,请回答下列问题。
溶液,请回答下列问题。
(1)应用托盘天平称取 晶体_______g。
晶体_______g。
(2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上(1g以下使用游码),天平平衡时,实际称量的 晶体是__________g。
晶体是__________g。
(3)本实验用到的主要仪器有:托盘天平、量筒、烧杯、玻璃棒、________、________。
(4)以下情况会使所配溶液的浓度产生何种影响(填“偏高”、“偏低”、“不变”。):
a.溶解晶体用的烧杯和玻璃棒未洗涤。____________
b.定容时俯视刻度线。____________
c.所用 晶体已失去部分结晶水。____________
晶体已失去部分结晶水。____________
(5)若 晶体中混有少量
晶体中混有少量 固体,且用所配制的
固体,且用所配制的 溶液与盐酸反应来测定某盐酸的物质的量浓度,所测盐酸的浓度会________。(填“偏高”、“偏低”、“不变”。)
溶液与盐酸反应来测定某盐酸的物质的量浓度,所测盐酸的浓度会________。(填“偏高”、“偏低”、“不变”。)
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H
②有关有机物的沸点:
| 试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
| 沸点/℃ |
34.7 |
78.5 |
118 |
77.1 |
请回答:(1)浓硫酸的作用是;
写出合成乙酸乙酯的化学方程式:
(2)球形干燥管C的作用是。
(3)饱和Na2CO3溶液的作用()
A.中和乙酸和乙醇.
B.中和乙酸并吸收部分乙醇.
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出.
D.加速酯的生成,提高其产率.
(4)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,
分离出;再加入(此空从下列选项中选择),然后进行蒸馏,收集77℃
左右的馏分,以得较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
为了检验和除去下表中的各种所含的杂质(括号里的物质),请从(I)中选出适当的
检验试剂,从(II)中选出适当的除杂试剂,将所选的答案的序号填入相应的空格内。
| 物质 |
检验试剂 |
除杂试剂 |
| 甲烷(乙烯) |
||
| 酒 精(水) |
(I)检验的试剂:
| A.无水硫酸铜 | B.酸性高锰酸钾溶液 | C.盐酸 | D.氢氧化钠溶液 |
(II)除杂试剂:a.硫酸 b.乙酸 c.新制的生石灰 d.溴水
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H
②有关有机物的沸点:
| 试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
| 沸点/℃ |
34.7 |
78.5 |
118 |
77.1 |
请回答:(1)浓硫酸的作用是 ;
写出合成乙酸乙酯的化学方程式:
(2)球形干燥管C的作用是 。
(3)饱和Na2CO3溶液的作用()
A.中和乙酸和乙醇.
B.中和乙酸并吸收部分乙醇.
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出.
D.加速酯的生成,提高其产率.
(4)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,
分离出 ;再加入(此空从下列选项中选择) ,然后进行蒸馏,收集77℃
左右的馏分,以得较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
为了检验和除去下表中的各种所含的杂质(括号里的物质),请从(I)中选出适当的
检验试剂,从(II)中选出适当的除杂试剂,将所选的答案的序号填入相应的空格内。
| 物质 |
检验试剂 |
除杂试剂 |
| 甲烷(乙烯) |
||
| 酒 精(水) |
(I)检验的试剂:
| A.无水硫酸铜 | B.酸性高锰酸钾溶液 | C.盐酸 | D.氢氧化钠溶液 |
(II)除杂试剂:a.硫酸 b.乙酸 c.新制的生石灰 d.溴水