(每空3分,共15分)原子序数依次增大 的四种常见元素W、X、Y、Z,均可形成一种或多种氧化物。其中W、Y的氧化物是导致酸雨的主要物质,X的氧化物既可以和强酸、亦可以和强碱反应,Z则具有砖红色和黑色的两
的四种常见元素W、X、Y、Z,均可形成一种或多种氧化物。其中W、Y的氧化物是导致酸雨的主要物质,X的氧化物既可以和强酸、亦可以和强碱反应,Z则具有砖红色和黑色的两 种氧化物。
种氧化物。 (1)W元素在元素周期表的位置为
(1)W元素在元素周期表的位置为  ,用电子式表示其气态氢
,用电子式表示其气态氢 化物 。
化物 。 (2)含有X的某种物质常用作净水剂,用离子方程式表示其净水的原理是
(2)含有X的某种物质常用作净水剂,用离子方程式表示其净水的原理是
。 (3)Y的一种氧化物,属于酸性氧化物,它既具有氧化性,也具有还原性,还具有漂白性。设计实验,验证该氧化物具有还原性,其操作方法是
(3)Y的一种氧化物,属于酸性氧化物,它既具有氧化性,也具有还原性,还具有漂白性。设计实验,验证该氧化物具有还原性,其操作方法是
 。
。
(4)一定物质的量的稀硝酸恰能将Z的砖红色的氧化物氧化,自身被还原成NO。则反应中氧化剂与还原剂的物质的量的比为 。
古代的“药金”外观与金相似,常被误认为金子。它的冶炼方法如下:将ZnCO3、赤铜(Cu2O)和木炭混合加热至800℃,得金光闪闪的“药金”,则药金的主要成分是________,有关的化学方程式是_______________、_______________、_______________。
用化学方程式表示下列反应,并注明反应属于四种基本反应类型中的哪一种?
(1)三氧化硫跟水反应
(2)加热高锰酸钾制氧气
(3)氧化铁跟盐酸反应
(4)氧化铜跟铝在高温下生成氧化铝和铜
向盛有氯气的三个集气瓶中,分别注入约五分之一的下列液体并振荡,观察下图所记录的现象,判断各瓶注入的液体是什么,将注入液体的编码填入图下方相应的括号中。
A.AgNO3溶液B.NaOH溶液C.水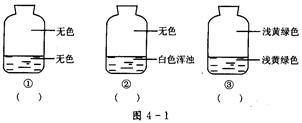
现有几种物质的熔点数据如下表:
| A组 |
B组 |
C组 |
D组 |
| 金刚石:3 550℃ |
Li:181℃ |
HF:-83℃ |
NaCl:801℃ |
| 硅晶体:1 410℃ |
Na:98℃ |
HCl:-115℃ |
KCl:776℃ |
| 硼晶体:2 300℃ |
K:64℃ |
HBr:-89℃ |
RbCl:718℃ |
| 二氧化硅1 723℃ |
Rb:39℃ |
HI:-51℃ |
CsCl:645℃ |
据此完成下列问题:
(1)A组属于_______________晶体,其熔化时克服的粒子间的作用力是_______________。
(2)B组晶体共同的物理性质是_______________ (填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于______________________________。
(4)D组晶体可能具有的性质是_______________ (填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)XY晶体的单元结构如下图所示,晶体中距离最近的X+与Y-的核间距离为a cm,已知阿伏加德罗常数为Na mol-1,其密度为ρ g·cm-3,则XY的摩尔质量可表示为________ g·mol-1。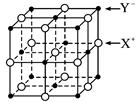
白磷分子中P—P键易断开,若一个白磷分子中每个P—P键断开插入一个氧原子,则一共可结合____________个氧原子,这样得到磷的一种氧化物,其分子式为________________。