有A、、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子, 比
比 少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1。请回答下列问题:
少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1。请回答下列问题:
(1)A单质、B单质、化合物R的熔点大小顺序为下列的 (填序号)。
①A 单质>B单质>R ②R>A单质>B单质
③B 单质>R>A单质 ④A单质>R>B单质
(2)在CB3分子中C元素原子的原子轨道发生的是________杂化,其固体时的晶体类型为 。
(3)写出D原子的核外电子排布式 _,C的氢化物比D的氢化物在水中溶解度大得多的可能原因 。
(4)右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体中阴、阳离子数之比为 ,FeD2物质中具有的化学键类型为 。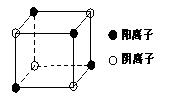
电解饱和食盐水装置的结构如图所示: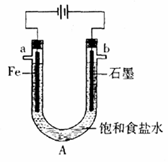
(1)写出电解食盐水的化学方程式
(2)滴入酚酞显红色的是极(填a或b,下同),___极产生的气体可使湿润的淀粉碘化钾试纸变蓝。
(3)工业上可以用生产的氯气制备漂白粉,该反应的化学方程式
在无土栽培中,配制1 L内含0.5 mol NH4Cl、0.16 mol KCl、0.24 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量分别为,,。
恒温下,a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)="13" mol,n(NH3)=" 6" mol,a=。
(2)反应达到平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量是。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始)∶n(平)=_________。
(4)原混合气体中,a∶b=_________。
(5)平衡混合气体中,n(N2)∶n(H2)∶n(NH3) =
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10 mol水消耗的能量是_____________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为;
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);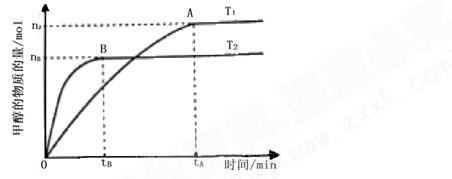
下列说法正确的是______(填序 号)
号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为 v(CH3OH)= 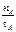 mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时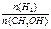 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为;
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为、正极的反应式为。
水的电离平衡如图所示.
(1)若A点表示25℃时水的电离平衡状态,当升高温度至100℃时水的电离平衡状态为B点,则此时水的离子积为
(2)将100℃时p H=8的Ba(OH)2溶液与pH=5的盐酸混合,并保持100℃的恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为
H=8的Ba(OH)2溶液与pH=5的盐酸混合,并保持100℃的恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为