A、B、C、D四种元素处于同一周期。在同族元素中,A的气态氢化物沸点最高,B的最高价氧化物对应水化物的酸性在同周期中最强,C的电负性介于A、B之间,D与B相邻。(1)C 原子的价电子排布式为___________________
原子的价电子排布式为___________________
(2)A、B、C三种原子的第一电离能由大到小的顺序是(写元素符号)_____ 。
(3)B的单质分子中存在① 个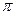 键;D的最简单气态氢化物分子中的中心原子轨道采用② 杂化。B和D形成一种超硬、耐磨、耐高温的化合物,该化合物属于③_______晶体,其硬度比金刚石
键;D的最简单气态氢化物分子中的中心原子轨道采用② 杂化。B和D形成一种超硬、耐磨、耐高温的化合物,该化合物属于③_______晶体,其硬度比金刚石
④ (填“大”或“小”)。
(4)A的气态氢化物的沸点在同族中最高的原因________ ____________________ 。
____________________ 。
用单线桥表示下列反应中原子间得失电子情况:5KI+KIO3+3H2SO4→3K2SO4+3I2+3H2O
对上述反应,__________发生了氧化反应,________元素被还原了,若有415g KI发生反应,则被还原的碘元素为________g,转移的电子数为__________mol。
隐形眼镜常用双氧水(即过氧化氢的水溶液)消毒,过氧化氢的分子式为H2O2,则在过氧化氢分子中存在的化学键类型有_________,过氧化氢属于_________(“离子”或者“共价”)化合物,过氧化氢的电子式为__________________。
四氯化碳是一种不溶于水且密度比水大的有机溶剂,现把溴从四氯化碳中除去,则可加入___________试液,充分振荡后,再用___________(填仪器名称)分离而得到纯净的四氯化碳,反应的化学方程式是________________________________。
食盐是重要的化工原料,电解饱和食盐水的化学方程式:________________________,电解食盐水中加入了几滴酚酞试液,接通电源,阳极产生____________,以____________试纸检验,还可以看到____________极附近的溶液变红,检验阴极气体的方法是______________。将其中两种产物化合又可以得到氯化氢,属于________(强、弱、非)电解质,将其溶于水后的电离方程式为__________________。
原电池的正极__________(填“得到”或“失去”)电子,发生__________(填“氧化”或“还原”)反应;负极__________(填“得到”或“失去”)电子,发生__________(填“氧化”或“还原”)反应。