某化学反应2A  B + D在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示。
B + D在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示。
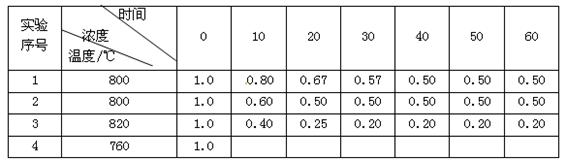
根据上述数据,回答下列问题:
(1)在实验1中,0~10min内的反应速率v(A)为 mol•L -1••min -1。
(2)与实验1相比,实验2的反应速率更 (填"快"或"慢"),其原因可能是 。
(3)根据实验1和实验3的数据分析升温对该反应的影响,写出两条结论:① ;
② 。
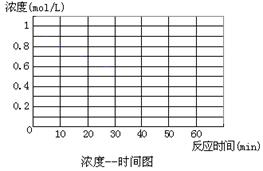
(4)实验4只改变温度,其它条件不变。请在答题卡的相应位置画出实验1和实验4的"浓度-时间"关系曲线。
某元素的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图为 。
据报道,某些花岗岩会产生放射性的氡 Rn),从而对人体产生伤害。请回答:
Rn),从而对人体产生伤害。请回答:
(1)该原子的质量数是 ,质子数是 ,中子数是 。
(2)请将以下Rn的原子结构示意图补全。
(3)请根据Rn的原子结构预测氡气的化学性质:
A.非常活泼,容易与氧气等非金属单质反应
B.比较活泼,能与钠等金属反应
C.不太活泼,与氮气性质相似
D.很难与其他物质发生反应
你选择 选项,理由是 。
(4)研究发现,镭能衰变为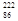 Rn,故称
Rn,故称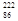 Rn为镭射气;钍能衰变为
Rn为镭射气;钍能衰变为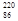 Rn,故将
Rn,故将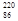 Rn称为钍射气;锕能衰变为
Rn称为钍射气;锕能衰变为 Rn,故将
Rn,故将 Rn称为锕射气
Rn称为锕射气 Rn
Rn Rn
Rn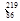 Rn是 (填字母序号)。
Rn是 (填字母序号)。
A.同种元素 B.同位素
C.同种核素 D.同种原子
请回答氯碱工业中的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=(要求写出计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是(填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中X、Y分别是、(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小;
②分别写出燃料电池B中正极、负极上发生的电极反应,正极:;负极:;
③这样设计的主要节(电)能之处在于(写出2处)、。
现代社会中铜在电气、交通、机械和冶金、能源及石化工业、高科技等领域有广泛的应用。某铜矿石含氧化铜、氧化亚铜、三氧化二铁和脉石(SiO2),现采用酸浸法从矿石中提取铜,其工艺流程图如下。其中铜的萃取(铜从水层进入有机层的过程)和反萃取(铜从有机层进入水层的过程)是现代湿法炼铜的重要工艺手段。
已知:①Cu+在酸性溶液中不稳定,可发生自身氧化还原反应;②当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;③反萃取后的水层2是硫酸铜溶液。
回答下列问题:
(1)矿石用稀硫酸处理过程中Cu2O发生反应的离子方程式为。
(2)“循环Ⅰ”经多次循环后的水层1不能继续循环使用,但可分离出一种重要的硫酸盐晶体,该晶体的化学式是。若水层1暴露在空气中一段时间后,可以得到另一种重要的硫酸盐,写出水层1暴露在空气中发生反应的离子方程式。
(3)写出电解过程中阳极(惰性电极)发生反应的电极反应式:。
(4)“循环Ⅲ”中反萃取剂的主要成分是。
材料是人类生存和社会进步的物质基础,不同的材料功能各不相同。以下都是有关材料的内容,试根据所给内容回答问题。
(1)氢能是未来能源最佳选择之一,氢能的利用涉及氢的储存、输送和使用。贮氢合金是解决氢的储存等问题的重要材料。贮氢合金中最具代表性的是镧镍合金(LaNi5),已知LaNi5(s)+3H2(g)=LaNi5H6(g) ΔH=-31.77 kJ·mol-1。
镧镍合金的熔点比镧、镍的熔点(填“高”、“低”或“介于两者之间”),根据反应原理,形成LaNi5H6的化学反应条件是。最近有人提出可以研制出一种性能优越的催化剂,可以大大提高贮氢合金的贮氢能力,你认为该讲法可信吗?(填“可信”或“不可信”),其理由是。
(2)无机非金属材料是日常生活中不可缺少的物质,它们往往具有高强度、耐高温、耐腐蚀的特点。Si3N4就是一种重要的精细陶瓷,合成氮化硅的方法之一为:3SiO2+6C+2N2 Si3N4+6CO。Si3N4属于晶体,在上述反应中氧化剂为。
Si3N4+6CO。Si3N4属于晶体,在上述反应中氧化剂为。
(3)有机高分子材料形式多样,ABS树脂广泛用于制造电讯器材、汽车、飞机零部件和各种仪器的外壳,它的结构可以表示为
试写出对应单体的结构简式CH2=CH—CN、、。
(4)高分子吸水树脂可以由聚乙烯醇(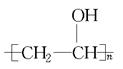 )和聚丙烯酸盐(
)和聚丙烯酸盐( )交联得到,从结构上看该高分子吸水材料具有吸水性,原因为它们都具有基团。
)交联得到,从结构上看该高分子吸水材料具有吸水性,原因为它们都具有基团。