下列关于SO2的说法,不正确的是
| A.SO2能使品红溶液褪色 | B.SO2能使紫色石蕊试液褪色 |
| C.SO2能与水作用生成H2SO3 | D.SO2是硫及其某些含硫化合物在空气中燃烧的产物 |
葛根素具有降血压等作用,其结构简式如下图,下列有关说法正确的是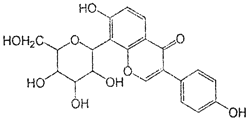
| A.该物质在一定条件下能发生消去反应、加成反应、取代反应 |
| B.葛根素的分子式为C21H22O9 |
| C.该物质一个分子中含有5个手性碳原子 |
| D.一定条件下1 mol 该物质与H2反应最多能消耗7 mol H2 |
下列说法中正确的是()
| A.常温下,某难溶物的Ksp为2.5×105 |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
C.NH3·H2O溶液加水稀释后,溶液中 的值增大 的值增大 |
| D.常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 |
短周期元素Q、W、X、Y、Z的原子序数依次增大,X元素的颜色反应呈黄色,Q原子的最外层电子数是其内层电子数的2倍,W、Z原子的最外层电子数相同,Z元素的核电荷数是W的2倍,Y是地壳中含量最多的金属元素。下列说法不正确的是()
| A.工业上常用电解的方法制备X、Y的单质 |
| B.元素Q和Z能形成QZ2型的共价化合物 |
| C.原子半径的大小顺序:r(X)> r(Y)> r(W)> r(Q) |
| D.元素X、Y的最高价氧化物对应的水化物之间能发生反应 |
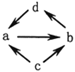
下列各组物质之间通过一步就能实现如图所示转化的是
| 物质编号 |
物质转化关系 |
a |
b |
c |
d |
| ① |
 |
Na2O |
Na2O2 |
Na |
NaOH |
| ② |
Al2O3 |
NaAlO2 |
Al |
Al(OH)3 |
|
| ③ |
FeCl2 |
FeCl3 |
Fe |
CuCl2 |
|
| ④ |
NO |
NO2 |
N2 |
HNO3 |
A.①② B.②③. C.②④ D.①③
下列指定反应的离子方程式正确的是
| A.氯化铝溶液中加入过量的氨水:Al3++4 NH3·H2O=AlO2-+4 NH4+ |
| B.稀硝酸中加入过量铁粉:Fe+4H++NO3-= Fe3++NO↑+2H2O |
| C.二氧化锰与浓盐酸混合加热:MnO2+4H++2Cl-△Mn2++ Cl2↑+2H2O |
| D.石灰水中加入过量小苏打溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |