现有A、B、C、D、E、F六种常见化合物 ,均为强电解质,它们的阳离子有Al3+、NH+4、Na+、Ag+、H+五种,阴离子有Cl-、HCO-3、OH-、NO-3、SO2-4五种,现将它们分别配成0.lmol/L。的溶液,进行如下实验:
,均为强电解质,它们的阳离子有Al3+、NH+4、Na+、Ag+、H+五种,阴离子有Cl-、HCO-3、OH-、NO-3、SO2-4五种,现将它们分别配成0.lmol/L。的溶液,进行如下实验:
①测得A溶液呈碱性,E溶液的pH为1,C溶液的酸性强于E溶液。
②向B溶液中滴入D溶液,出现白色沉淀和无色无味气体,该白色沉淀既能溶于A溶液,又能溶于C溶液;过滤,向滤液中加入A溶液,加热,有刺激性气味气体产生。
③向B溶液中滴加F溶液,产生白色沉淀,加入过量E溶液,沉淀不溶解。
④向E溶液中滴加F溶液,无明显变化。
根据上述实验现象,回答下列问题:
(1)写出下列四种化合物的化学式:
A 、B 、D 、F 。
(2)C溶液是 ,判断依据是____
(3)B、D反应的离子方程式是____ ;
某些化学反应可用下式表示A+B→→C+D+H2O。请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式: 。
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是 。
(3)若A、C均含有铝元素。①当B是盐酸时,C是 ;
②当B是NaOH时,C是 。
含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、Na2SO4这7种常见的含硫化合物。回答下列问题:
(1)写出硫元素在周期表中位置______________
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子反应方程式 。
(3)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面 ,则发生了钝化。
(4)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。该反应的化学方程式: 。
下列物质中互为同分异构体的有,互为同素异形体的有,属于同位素的有,属于同一种物质的有。(填序号)
①液氯 ②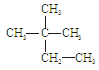 ③白磷 ④18O ⑤
③白磷 ④18O ⑤
⑥红磷⑦16O⑧氯气
(14分)某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应。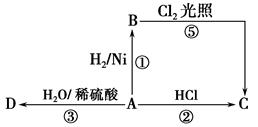
据图回答下列问题:
(1)写出A、C、D的结构简式:A________, C________, D________。
(2)写出①②两步反应的化学方程式,并注明反应类型:
①________________________________________________反应类型为 ____________。
②_______________________________________________
(8分)有机物M的结构简式如图所示。
(1)有机物M的苯环上的一氯代物有________种。
(2)1 mol M与足量溴水混合,消耗Br2的物质的量为________mol。
(3)1 mol M与足量H2加成,消耗H2________ mol。
(4)下列有关M的说法中不正确的是________。
| A.在催化剂的作用下,M可与液溴发生取代反应 |
| B.M使溴水褪色的原理与乙烯使溴水褪色的原理相同 |
| C.M能使酸性KMnO4溶液褪色 |
| D.M的分子式为C15H16 |