硬质玻璃管是化学实验中经常使用的一种仪器,分析下列实验(固定装置及尾气处理过程均略去)并回答:
(1)如图所示,通入C12—段时间后,观察A、B、C三个棉球的变化,并补充完成下表所示的实验报告。
| 实验内容 |
实验现象 |
解释或结论 |
|
| 棉 球 |
棉球上滴加试剂 |
||
| A |
KBr溶液 |
棉球变为___________色 |
化学方程式:__________ |
| B |
_____溶液 |
棉球变为棕黄色 |
离子方程式:__________ |
| C |
淀粉溶液 |
①棉球变为蓝色; ②待试管冷却后,在B、C之间的玻璃壁上有_____色固体产生 |
②的原因:__________ |
(2)实验室里,氯气通常用浓盐酸和二氧化锰在加热的条件下制取,该反应的化学方程
式为______________________________,此外还可以用高锰酸钾、氯酸钾等氧化剂与浓盐酸在常温下反应制取。某化学课外活动小组用如图所示的装置制取氯气并模拟盐酸工 业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸)。
业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸)。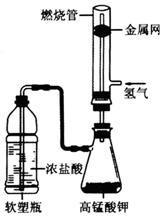
实验过程如下:
步骤一:先通入氢气,验纯后点燃;
步骤二:待氢气稳定燃烧后,挤压软塑瓶,将浓盐酸加入锥形瓶中,氢气持续安静燃烧。
请回答:
①步骤二完成后,火焰的颜色由淡蓝色变为__________色,燃烧管的上方可观察到_____现象;
②先通氢气并点燃,再通氯气的原因是_______________
③采用外管通氢气、内管通氯气的目的是______________ ______。
______。
请设计CO2在高温下与木炭反应生成CO的实验。
(1)在下面方框中,A表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置,连接胶 管及尾气处理部分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如下:
管及尾气处理部分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如下: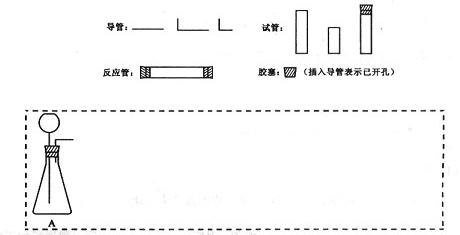
(2)根据方框中的装置图,在答题卡上填写该表
| 仪器符号 |
仪器中所加物质 |
作用 |
| A |
石灰石、稀盐酸 |
石灰石与盐酸生成CO2 |
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是________________________;
(4)验证CO的方法是____________________________;
以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。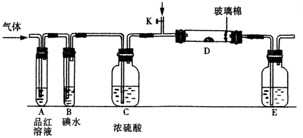
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?(填“相同”或“不相同”);若置D装的是铁粉,通入Cl2与铁粉充分反应时现象为
;若装置D中装的是五氧化二钒(催化剂)。通入SO2时,打开K通入适量O2的化学反应方程式为。
②若装置B中装有5.0 mL 1.0×10-3mol/L在碘水,当通入足量Cl2完全反应后,共转移了5.0×10-5mol电子,该反应的化学方程式为。
③E中盛有溶液。
(2)某同学将足量的SO2通入一支装有氧化钡溶液的试管,未见沉淀生成,若向该试管中加入加量(填字母),则可以看到白色沉淀产生。
| A.氨水 | B.稀盐酸 | C.稀硝酸 | D.氯化钙 |
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4∶3;当Cl2的与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式。
某同学想通过比较两种最高价氧化物对应水化物的酸性强弱来验证硫与碳的非金属性的强弱,他采用了如图所示的装置。请回答: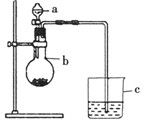
(1)仪器a的名称是,应盛放下列药品中的。
A.稀硫酸 B.亚硫酸
C.氢硫酸 D.盐酸
(2)仪器b的名称是,应盛放下列药品中的。
A.碳酸钙 B.硫酸钠
C.氯化钠 D.碳酸钠
(3)如果观察到C中的现象为,即可证明硫与碳的非金属性的强弱。
(9分) 四氯化钛是无色液体,沸点为136℃。它极易水解,遇空气中水蒸气即产生“白烟”(TiCl4+H2O=TiOCl2+2HCl↑),在650℃~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。下图是实验室制备TiCl4的反应装置,其主要操作步骤如下:
①连接好整套装置,在通Cl2前先通入CO2气体并持续一段时间;
②当锥形瓶中TiCl4的量不再增加时,停止加热,从侧管中改通CO2气体直到电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④ 将电炉升温到800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水。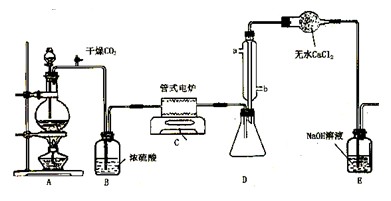
试回答下列问题:
(1)正确的操作顺序为(填序号)。
(2)装置A中的反应的离子方程式为。
(3)C装置中的反应方程式为:。
(4)操作①的目的是。
(5)装置D中冷凝管进水口的位置是(填a或b),装置E的作用是。
为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。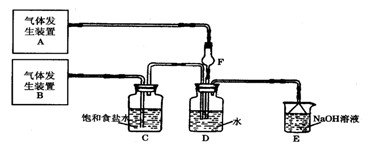
试填空。
(1)D装置中主要反应的离子方程式为,
F仪器的作用是:。
(2)为验证通入D装置中气体是Cl2还是SO2过量,兴趣小组的同学准备了以下试剂: ① 氯化铁稀溶液 ② 氯化亚铁溶液 ③ 硫氰化钾溶液
① 氯化铁稀溶液 ② 氯化亚铁溶液 ③ 硫氰化钾溶液
④ 苯酚溶液 ⑤ 品红溶液 ⑥ 酸性高锰酸钾溶液
若Cl2过量:取适量D中溶液滴加至盛有(选填一个序号)试剂的试管内,再加入(选填一个序号)试剂,发生的现象是:;
若SO2过量:取适量D中溶液滴加至盛有(选填一个序号)试剂的试管内,发生的现象是:。