储存浓H2SO4 的铁罐外口会出现严重的腐蚀现象,这体现浓H2SO4的
| A.吸水性和酸性 | B.脱水性和吸水性 |
| C.强氧化性和吸水性 | D.不挥发性和酸性 |
下列说法中正确的是
| A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同 |
B.某金属阳离子的结构示意图为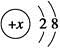 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 |
C.二硫化碳是直线形非极性分子,其电子式为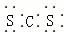 |
| D.中子数为18的氯原子可表示为18Cl |
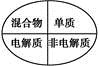
下列逻辑关系图示中正确的是
| A |
B |
C |
D |
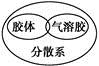 |
 |
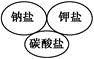 |
 |
下列有关物质组成、性质和变化的说法中,正确的是
| A.化学变化不产生新元素,产生新元素的变化不是化学变化 |
| B.石油的分馏、裂化、裂解和煤的干馏都属于化学变化 |
| C.导电性属于物质的物理性质,所以物质导电时不可能发生化学变化 |
| D.某微粒的电子数等于质子数,则该微粒可能是分子或离子 |
在一定温度下,已知有关某溶液的一些数据:①溶液的质量②溶剂的质量 ③溶液的体积 ④溶质的摩尔质量 ⑤溶质(气体)的体积(Vm已知) ⑥溶液的密度 ⑦溶液的质量分数。利用下列各组数据计算该溶液的物质的量浓度,不能算出的一组是
| A.③⑤ | B.②④⑤⑥ | C.①④⑥ | D.①②③④ |
某同学用NaHCO3和KHCO3组成的固体混合物进行实验,测得实验数据(盐酸的物质的量浓度相等)如表所示:下列说法不正确的是
| 盐酸/mL |
50 |
50 |
50 |
| 固体混合物质量/g |
9.2 |
15.7 |
27.6 |
| 标准状况下CO2体积/L |
2.24 |
3.36 |
3.36 |
A.盐酸的物质的量浓度为3.0 mol/L
B.根据表中数据能计算出混合物中NaHCO3的质量分数
C.加入9.2 g固体混合物时盐酸过量
D.15.7 g固体混合物恰好与盐酸完全反应