下列排列顺序正确的是
①固体热稳定性:Na2CO3>CaCO3>NaHCO3
②微粒半径:F->Na+>Mg2+>S2-
③燃烧热: S(气体)>S(液体)>S(固体)
④物质的熔点:植物油>动物油
| A.①③④ | B.①③ | C.①②③④ | D.②③④ |
下列各组反应中,所得产物相同的是
A.金属钠在常温或加热时与氧气反应 |
B.氯化铝溶液与少量氨水或过量氨水反应 |
C.金属铜与浓硝酸或稀硝酸反应 |
D.溴乙烷与烧碱的水溶液或烧碱的醇溶液反应 |
下列做法不利于环境保护的是
| A.将煤液化或气化获得清洁燃料 |
| B.研发燃料电池替代铅酸蓄电池 |
| C.使用简易布袋代替塑料购物袋 |
| D.用性质稳定的氟利昂作致冷剂 |
钡和钠相似,也能形成O22–离子的过氧化物,则下列叙述错误的是()
A.1mol过氧化钠或过氧化钡跟足量水反应都生成0.5mol氧气 |
B.过氧化钡的化学式是Ba2O2 |
C.过氧化钡是离子化合物 |
D.过氧化钠和过氧化钡都是强氧化剂 |
在一定体积的密闭容器中放入3升气体R和7升气体Q,在一定条件下发生反应:3R(气)+5Q(气)="=" 4X(气)+nY(气)反应完全后,容器温度不变,混和气体的压强是原来的110%,则化学方程式中的n值是:
| A.2 | B.3 | C.4 | D.5 |
两个原硅酸分子的OH原子团之间可以相互作用而脱去一分子水:
2H4SiO4===H6Si2O7+H2O,原硅酸结构为: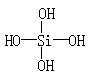 , 则在所得的H6Si2O7分子的结构中,含有的硅氧键数目为()
, 则在所得的H6Si2O7分子的结构中,含有的硅氧键数目为()
| A.5 | B.6 | C.7 | D.8 |