已知:苯环上连有的基团不同时,新的基团可能进入间位,也可能进入邻、对位。
煤是非再生能源,我国煤炭储量占能 源总储量约94%。下图是煤干馏得到的主要产物,以及产物之一甲苯的有关反应。回答下列问题:
源总储量约94%。下图是煤干馏得到的主要产物,以及产物之一甲苯的有关反应。回答下列问题:
(1)煤的干馏是指 。固态物质A是 (写名称),它是冶金工业的重要原料,还用于 (再写一种用途)。
(2)由甲苯制备物质C时,若反应①和②的顺序交换,得到的物质不是C,而可能是
(写结构简式,一种即可)。
(3)反应③的反应条件是 ;反应④是 反 应(填反应类型)。
应(填反应类型)。
(4)与E含相同基团(苯基和—C≡C—)的E的同分异构体(包括E)共 种。
发生化学反应时,破坏化学键需要能量,形成化学键需要能量。吸收能量用E1表示,释放能量用E2表示,当E1E2时,反应吸收能量;当E1E2时,反应释放能量
工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体: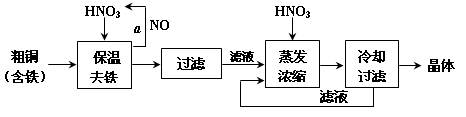
(1)在步骤a中,还需要通入氧气和水,发生反应的化学方程式是
。
(2)在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在范围。若调节溶液的pH=4,此时,溶液中c (Fe3+) =。[已知该条件下,Fe(OH)3的KSP= 4.0×10-36 ]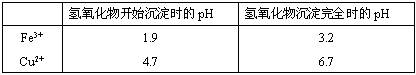
(3)不用加水的方法调节溶液pH的原因是。
(4)进行蒸发浓缩时,要加适量的硝酸以保持溶液一定的c(H+),其目的是(结合离子方程式简要说明)。
(5)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是。
[化学——有机化学基础]
Ⅰ.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛。结构简式如图。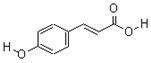
(1)该有机物具有的官能团名称是(写出其中的两种)。
(2)该有机物能发生的反应类型是(填写代号)。
A.氧化反应 B.消去反应 C.加聚反应 D.水解反应
Ⅱ.芳香族化合物C10H10O2有如下的转化关系: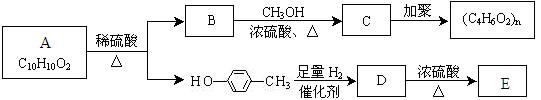
已知E能使Br2/CCl4溶液褪色。请回答下列问题:
(3)请分别写出A、E的结构简式A E。
(4)若有机物F与C互为同分异构体,则与有机物B为同系物的F的同分异构体有种
(5)请写出B→C反应的化学方程式。
[化学——物质结构与性质]
已知A、B、C、D、E五种元素的原子序数依次增大,其中A、E原子的最外层电子数均等于其周期序数,E原子的电子层数是A的3倍;B原子核外电子有6种不同的运动状态,S轨道电子数是P轨道电子数的两倍;D原子L层上有2对成对电子。请回答下列问题:
(1)E元素基态原子的电子排布式为。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为(填元素符号)。
(3)D元素与氟元素相比,电负性:DF(填“>”、“=”或“<”)。
(4)BD2在高温高压下所形成的晶体其晶胞如图所示。该晶体的类型属于(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子轨道的杂化类型为。l mol B2A2分子中含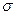 键的数目是。
键的数目是。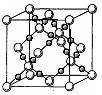
(5)光谱证实单质E与强碱溶液反应有[E(OH)4]—生成,则[E(OH)4]—中存在。
a.共价键 b.配位键 c.σ键 d.π键
物质A、B、C有如下转化关系: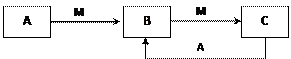
请回答下列问题:
(1)若A、B、C均为含铝元素的化合物,M可以是 。
(2)若M是第IVA族某元素的最高价氧化物,且M为气体,组成A的阴阳离子均含有10个电子,请写出C的名称 
(3)若A是一种黄绿色气体,M是一种常见金属。写出C→B的离子方程式
。
(4)若A、B、C都是含硫化合物,已知:
A转化为B的热化学方程式:2H2S(g)+ O2(g) =2S (s)+2H2O(l) △H= -a kJ·mol-1;
A转化为C的热化学方程式:2H2S(g)+ 3O2(g) =2SO2(g)+2H2O(l) △H= -b kJ·mol-1;
请写出A与C反应转化为B的热化学方程式。
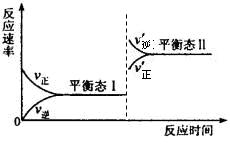
(5)若C+A→B的转化关系为4NH3+6NO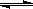 6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系如图。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)
6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系如图。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)