对于Zn(s)+H2SO4(aq)== ZnSO4(aq)+H2(g)的化学反应(反应放热),下列叙述一定正确的是
| A.若将该反应设计成原电池,锌为负极,发生还原反应 |
| B.1 mol锌的能量高于1 mol H2所含的能量 |
| C.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L |
| D.反应过程中的能量关系可用右图表示 |
下列与金属腐蚀有关的说法,正确的是 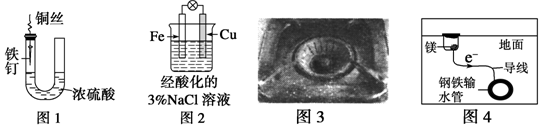
| A.图1中,铁钉易被腐蚀 |
| B.图2中,滴加少量KSCN溶液,溶液变为血红色 |
| C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 |
| D.图4中, 用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
下列有关试剂的保存方法,错误的是
| A.浓硝酸保存在无色玻璃试剂瓶中 |
| B.少量的钠保存在煤油中 |
| C.氢氧化钠溶液保存在具橡皮塞的玻璃试剂瓶中 |
| D.新制的氯水通常保存在棕色玻璃试剂瓶中 |
下列推断正确的是
| A.绿色化学的核心是应用化学原理对环境污染进行治理 |
| B.硅是地壳中含量位居第二的元素,玛瑙、光导纤维的主要成分为SiO2 |
| C.配制240 mL 1 mol·L-1的NaOH溶液需称NaOH固体的质量为9.6 g |
| D.要除去衣服上的顽固污渍,均可将衣服泡在漂白液中 |
化学与生产、生活密切相关。下列说法正确的是
| A.对“地沟油”进行分馏可以获得汽油发动机的燃料 |
| B.用纯碱制玻璃、用铁矿石炼铁都会产生温室气体 |
| C.海水中有大量人类需要的物质,可以大量开发海水中的物质,以解决资源短缺的问题 |
| D.工业上以氯气和澄清石灰水为原料制造漂白粉 |
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol·L-1和2mol·L-1,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下气体的体积为(设反应中HNO3被还原成NO)
| A.0.448L | B.0.672L | C.0.896L | D.0.224L |