下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
恒温恒容下,向2 L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g)
MgO(s)+CO2(g)+SO2(g)
反应过程中测定的部分数据见下表:
| 反应时间/min |
n(MgSO4)/mol |
n(CO)/mol |
n(SO2) / mol |
| 0 |
2.0 |
2.0 |
0 |
| 2 |
0.8 |
||
| 4 |
1.2 |
||
| 6 |
1.2 |
2.8 |
下列说法正确的是
A.0~2 min内的平均速率为υ (CO)=0.6 mol/(L·min)
B.4 min后,平衡移动的原因可能是向容器中加入了2.0 mol的SO2
C.4 min后,若升高温度,SO2物质的量浓度变为0.7mol/L,则正反应为放热反应
D.其他条件不变,若起始时容器中MgSO4、CO均为1.0 mol,则平衡时n(SO2)="0.6" mol
依据下列实验现象,得出的结论正确的是
| 选项 |
操作 |
实验现象 |
结论 |
| A |
向NaBr溶液中加入氯水,再加入淀粉KI溶液 |
溶液变蓝 |
氧化性:Cl2>Br2>I2 |
| B |
将铝片放入盐酸中 |
产生气泡的速率先慢后快,再逐渐减慢 |
H+的浓度是影响反应速率的唯一因素 |
| C |
向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜加热 |
得到蓝色溶液 |
蔗糖水解产物没有还原性 |
| D |
向漂白粉中滴入稀硫酸,将生成的气体通入品红溶液 |
品红溶液褪色 |
气体中含有Cl2 |
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如下图。下列说法不正确的是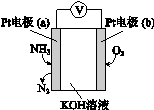
| A.O2在电极b上发生还原反应 |
| B.溶液中OH—向电极a移动 |
| C.反应消耗的NH3与O2的物质的量之比为4:5 |
| D.负极的电极反应式为:2NH3-6e-+6OH-=N2+6H2O |
下列关于反应能量的说法正确的是
| A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)ΔH="-216" kJ·mol-1,反应物总能量<生成物总能量 |
| B.相同条件下,1 mol氢原子所具有的能量为E1,1 mol 氢分子的能量为E2,则2E1>E2 |
| C.已知2H2(g)+O2(g)= 2H2O(g)ΔH="-483.6" kJ·mol-1, H2的燃烧热为241.8 kJ·mol-1 |
| D.H+(aq)+OH-(aq)= H2O(l) ΔH="-57.3" kJ·mol-1,含1 mol NaOH的NaOH溶液与含 |
0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ 的热量
下列解释事实的化学方程式不正确的是
| A.金属钠在空气中加热,生成淡黄色固体:2Na+O2△Na2O2 |
| B.向硫酸铝溶液中加入氨水制备氢氧化铝:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
| C.铁在潮湿的环境中生锈:3Fe+4H2O= Fe3O4+4H2↑ |
| D.二氧化氮溶于水有硝酸生成:3NO2+H2O=2HNO3+NO |