(1)某种苯的同系物0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。实践中可根据核磁共振氢谱(PMR)上观察到氢原子给出的峰值情况,确定有机物 的结构。此含有苯环的有机物,在PMR谱上峰给出的稳定强度仅有四种,它们分别为:① 3∶1∶1 ②1∶1∶2 ∶6 ③3∶
的结构。此含有苯环的有机物,在PMR谱上峰给出的稳定强度仅有四种,它们分别为:① 3∶1∶1 ②1∶1∶2 ∶6 ③3∶ 2 ④3∶2∶2∶2∶1 ,请分别推断出其对应的结构:
2 ④3∶2∶2∶2∶1 ,请分别推断出其对应的结构:
① ; ② ;
③ ; ④ 。
(2)下表中括号内物质为所含的少量杂质,请选用适当的试剂和分离装置将杂质除去,并将所选的试剂及装置的编号填入表中。
试剂:①水;②氢氧化钠;③溴水;④酸性高锰酸钾
分离装置:A、分液装置;B、蒸馏装置;C、洗气装置;
| |
需加入的试剂 |
分离装置 |
| 乙烷(乙烯) |
|
|
| 乙醇(乙酸) |
|
|
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。
从废料中回收氧化钴(CoO)的工艺流程如下:
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为。
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为(产物中只有一种酸根)。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因_______________。
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式____________________。
(4)碳酸钠溶液在过程III和IV中所起作用有所不同,请写出在过程IV中起的作用是__________。
(5)在Na2CO3溶液中存在多种粒子,下列各粒子浓度关系正确的是______(填序号)。
| A.c(Na+) = 2c(CO32-) |
| B.c(Na+) > c(CO32-) > c(HCO3-) |
| C.c(OH-) > c(HCO3-) > c(H+) |
| D.c(OH-) - c(H+) = c(HCO3-) + 2c(H2CO3) |
(6)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。下图是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,A物质的化学式是______。
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
(1)工业上制备ClO2的反应原理常采用:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
① 浓盐酸在反应中显示出来的性质是_______(填序号)。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
② 若上述反应中产生0.1 mol ClO2,则转移电子的物质的量为_______mol。
(2)目前已开发出用电解法制取ClO2的新工艺。
①上图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式:__________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为_________mol;用平衡移动原理解释阴极区pH增大的原因______________。
(3)ClO2对污水中Fe2+、Mn2+、S2—和CN-等有明显的去除效果。某工厂污水中含CN- a mg/L,现用ClO2将CN-氧化,只生成两种气体,其离子反应方程式为_______;处理100 m3这种污水,至少需要ClO2 _______ mol 。
X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大。有关信息如下表:
| X |
动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y |
地壳中含量居第一位 |
| Z |
短周期中其原子半径最大 |
| Q |
生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M |
海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式____________。
(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族。下列有关说法正确的是____________(填序号)。
A.原子半径: Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)化合物QX导热性好,热膨胀系数小,是良好的耐热冲击材料。抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料。有关化合物QX的制备及化学性质如下(所有热量数据均已折合为25℃、101.3 kPa条件下的数值)
可用Q和X的单质在800 ~ 1000℃制得,每生成1 mol QX,吸收a kJ的热量。
可用Q的氧化物、焦炭和X的单质在1600 ~ 1750℃生成QX,每生成1 mol QX,消耗18 g碳,吸收b kJ的热量。
请根据上述信息写出在理论上Q的氧化物跟焦炭反应生成Q单质和CO的热化学方程式________________。
(4)X、Y组成的一种无色气体遇空气变为红棕色。将标准状况下40 L该无色气体与15 L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐。请写出该反应的离子方程式。
以烯烃为原料,合成某些高聚物的路线如下: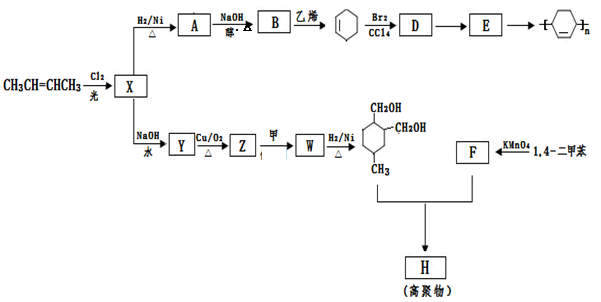
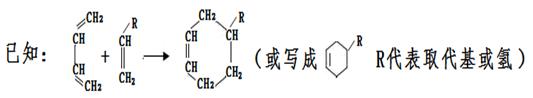
(1)CH3CH=CHCH3的名称是。
(2)X中含有的官能团是。
(3)A→B的化学方程式是。
(4)D→E的反应类型是。
(5)甲为烃,F能与NaHCO3反应产生CO2。
① 下列有关说法正确的是。
a.有机物Z能发生银镜反应 b.有机物Y与HOCH2CH2OH 互为同系物
c.有机物Y的沸点比B低 d.有机物F能与己二胺缩聚成聚合物
② Y的同分异构体有多种,写出分子结构中含有酯基的所有同分异构体的结构简式。
③ Z→W的化学方程式是。
(6)高聚物H的结构简式是。
由废铁制备FeCl2的主要过程如下:
Ⅰ.按下图所示过程制备FeCl3•6H2O 
(1)①中产生气体的电子式是。
(2)用离子方程式表示过程②中稀硝酸的作用,在该过程中要不断向溶液中补充盐酸,目的是。
Ⅱ.由FeCl3 • 6H2O制得干燥FeCl2的过程如下:
ⅰ.向盛有FeCl3 • 6H2O的容器中加入SOCl2,加热,获得无水FeCl3
ⅱ.将无水FeCl3置于反应管中,通入①中产生的气体一段时间后加热,生成FeCl2
ⅲ.收集FeCl2,保存备用
(3) SOCl2与水接触会迅速产生白雾和SO2。加热分解FeCl3 • 6H2O不能得到无水FeCl3,而步骤ⅰ中可得到无水FeCl3,结合必要化学方程式解释得到无水FeCl3的原因。
(4)过程ⅱ中产生FeCl2的化学方程式是。
Ⅲ.FeCl2的包装上贴有安全注意事项,部分内容如下:
| 品 名 |
氯化亚铁 |
| 理化特性 |
白色,遇空气易变成黄色,易吸水,有腐蚀性…… |
| 注意事项 |
避免接触空气、碱等;聚乙烯塑料桶包装;避免受热 |
(5)下列说法正确的是。
a.密闭保存、远离火源
b.可以与强氧化剂共同存放、运输
c.不宜用铁制容器包装而要用聚乙烯塑料桶包装
(6)FeCl2在空气中受热可生成氯化铁、氧化铁等,反应的化学方程式是。