一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体。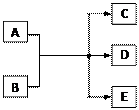
(1)若A、C、D均含氯元素,C为氯碱工业的原料,
D溶液具有漂白性,则A与B反应的化学方程式是 ;D溶液可使KI淀粉溶液显蓝色,则D与KI在溶液中反应的离子方程式是 ;过量B溶液与NH4HCO3溶液共热,生成气体G的离子方程式是 ,G遇硝酸蒸气的现象是 。
(2)若A为红色金属,B为某酸的浓溶液,D可形成酸雨的无色气体。A与B反应的化学是 ;a molA与足量的B充分反应后,将产生的D通入NaOH溶液中,恰好完全反应,则所需NaOH的物质的量的范围是 。
(3)上述(1)、(2)中的D都能使品红溶液褪色,利用褪色后的溶液,探究使品红溶液褪色的物质的实验方法是 。
(16分) 碳及其化合物有广泛的用途。
(1)反应C(s)+ H2O(g)  CO(g) +H2(g)ΔH=" +131.3" kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是。
CO(g) +H2(g)ΔH=" +131.3" kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是。
| A.增加碳的用量 | B.升高温度 | C.用CO吸收剂除去CO | D.加入催化剂 |
(2)已知,C(s)+ CO2(g) 2CO(g) △H=+172.5kJ•mol-1
2CO(g) △H=+172.5kJ•mol-1
则反应 CO(g)+H2O(g) CO2(g)+H2(g)的△H=kJ•mol-1。
CO2(g)+H2(g)的△H=kJ•mol-1。
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
| t / min |
2 |
4 |
7 |
9 |
| n(H2O)/mol |
0.12 |
0.11 |
0.10 |
0.10 |
①其它条件不变,降低温度,达到新平衡前v(逆)_____v(正)(填“>”、“<”或“=”) 。
②该温度下,此反应的平衡常数K=__________;
③其它条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数______(填“增大”、“减小”或“不变”)。
某新型液晶有机物基元IV的合成线路如下: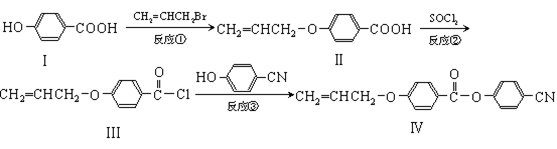
(1)Ⅰ的分子式,Ⅰ中含氧官能团的名称,反应①的类型为反应。
(2)CH2=CHCH2Br与NaOH水溶液反应的化学方程式(注明条件)。
(3)II可发生加聚反应,所得产物的结构简式。
(4)有关化合物Ⅰ和II的说法中,不正确的是。
| A.1molⅠ充分燃烧需要消耗6mol O2 | B.1molⅠ最多可消耗2mol NaOH |
| C.II能使溴的CCl4溶液褪色 | D.II能使酸性KMnO4溶液褪色 |
(5)一定条件下, 也可与III发生类似反应③的反应,生成有机物V,V的结构简式是。
也可与III发生类似反应③的反应,生成有机物V,V的结构简式是。
(6)化合物I的同分异构体中,苯环上一溴代产物只有两种,遇FeCl3溶液显紫色,还能发生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式。
(12分)
碳、硫的含量影响钢铁性能。碳、硫含量的一种测定方法是将钢样中的碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下将x g钢样中的碳、硫转化为CO2、SO2。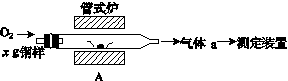
①气体a的成分是______。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5O2 1________+3________。
1________+3________。
(2)将气体a通入测硫装置中(如图),采用滴定法测定硫的含量。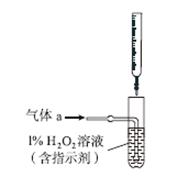
①H2O2氧化SO2的化学方程式:__________________。
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液。若消耗1 mL NaOH溶液相当于硫的质量为y g,则该钢样中硫的质量分数:________。
(3)将气体a通入测碳装置中(如图),采用重量法测定碳的含量。
①气体a通过B和C的目的是________________________________________。
②计算钢样中碳的质量分数,应测量的数据是_________________________。
(12分)已知A、B、C、D、E、F、G都是短周期的元素,它们的原子序数依次递增.A原子的电子层数与它的核外电子总数相同,而B原子的最外层电子数是次外层的2倍,C的氢化物可使湿润的红色石蕊试纸变蓝,B和D可以形成两种气态化合物,E原子核外电子总数比B的2倍少1,D与F同主族,G的原子半径是本周期元素中最小的.则:
(1)运送飞船的火箭燃料有一种液态化合物是由A、C元素组成的,已知该化合物的相对分子质量为32,其中氢元素的质量分数为12.5%.若该化合物与A2D2恰好完全反应,能产生两种无毒又不污染环境的物质,试写出该反应的化学方程式:__________________。
(2)C的原子间也可形成链状结构,假设C原子间只以单键形式连接,并与A形成系列化合物,则该系列化合物的通式为___________________________。
(3)由B和D以质量比为3∶8组成的化合物与E的同周期相邻主族元素的单质反应的化学方程式为________________________________________。
(4)F单质与E的最高价氧化物的水化物反应的离子方程式为_____________________。
N元素有多种化合物,它们之间可以发生转化,如:N2H4+HNO2=2H2O+HN3。请回答下列问题:
(1)N与O电负性较大的是。
(2)NaN3的晶体类型是。
(3)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8K,主要原因是。
(4)N2H4中的N原子的杂化类型是。
(5)NO2-离子是一种很好的配位体,能提供孤电子对是。
A.氧原子 B.氮原子 C.两者都可以
NO2-与钴盐通过配位键形成的[Co(NO2)6]3-能与K+离子结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+离子,写出该配合物中钴离子的电子排布式。