已知H2(g)+Br2(l)=2HBr(g),1gH2完全反应放出热量是36KJ ,已知H2(g)的键能是436KJ/mol,HBr(g)的键能是369KJ/mol,则Br2(l)的键能是
| A.404 KJ/mol | B.260 KJ/mol | C.230 KJ/mol | D.200 KJ/mol |
电瓶车所用电池一般为铅蓄电池(如图),这是一种典型的可充电电池,电池总反应式为: Pb+PbO2+2H2 SO4 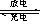 2Pb SO4+2H2O。则下列说法正确的是
2Pb SO4+2H2O。则下列说法正确的是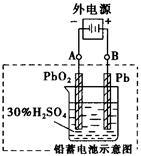
| A.放电时,负极板上发生了还原反应 |
| B.放电时,正极反应是:Pb一2e一+ SO42—=PbSO4 |
| C.充电时,铅蓄电池的负极应与充电器电源的正极相连 |
| D.充电时,阳极反应是:PbSO4一2e一+2H2O= PbO2+ SO42—+4H+ |
如图所示,电流计的指针发生偏转,正极变粗,负极变细,符合这种情况的是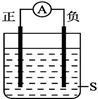
| A.正极Cu,负极Zn,S为稀H2SO4 |
| B.正极Zn,负极Cu,S为CuSO4溶液 |
| C.正极Ag,负极Zn,S为AgNO3溶液 |
| D.正极Fe,负极Cu,S为AgNO3溶液 |
下列用来表示物质变化的化学用语中,正确的是
| A.氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e一=4OH- |
| B.电解饱和食盐水时,阳极的电极反应式为:2C1-一2e一 =C12↑ |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极主要反应式为:Cu一2e-=Cu2+ |
| D.钢铁发生电化学腐蚀的负极反应式:Fe一3e—=Fe3+ |
今有如下三个热化学方程式:
H2(g)+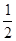 O 2(g)=H2O(g) ΔH=a kJ·mol-1;
O 2(g)=H2O(g) ΔH=a kJ·mol-1;
H2(g)+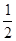 O 2(g)=H2O(l) ΔH=b kJ·mol-1;
O 2(g)=H2O(l) ΔH=b kJ·mol-1;
2H2(g)+O2(g)=2H2O(l) ΔH=c kJ·mol-1。
关于它们的下列表述正确的是
| A.三个都是吸热反应 | B.a、b、c均为正值 |
| C.a=b | D.2b=c |
关于下图所示的原电池,下列说法正确的是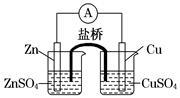
| A.电子沿着盐桥从锌电极流向铜电极 |
| B.盐桥中的阳离子向硫酸铜溶液中迁移 |
| C.电流从锌电极通过电流计流向铜电极 |
| D.铜电极上发生的电极反应是2H++2e-===H2↑ |