煤的直接燃烧已引起严重的生态和环境污染,并且其直接燃烧很难解决温室气体减排问题。解决煤炭的清洁高效利用问题是中国发展低碳经济的关键。下图是煤气化和除硫的实验系统示意图: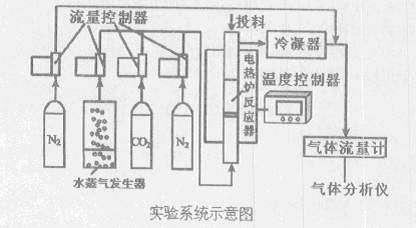
其操作步骤为:
I.升温至实验温度,通人高纯N2,从投料口加人石英砂(含载氧体)
Ⅱ.停止通入N2,从反应器下方按比例通入水蒸气和CO2,从投料口加入CaO
Ⅲ.停止通入水蒸气和CO2,从投料口加入煤
Ⅳ.持续通入水蒸气和CO2,开始反应;在气体出口管中通人高纯N2
(1)冷凝器的作用是 。
(2)可使用CaCO3代替CaO脱硫,CaCO3脱硫的化学方程式为 。
(3)通人N2的目的: 。
(4)反应器中发生如下几种反应:
C(s)十H2O(g)=CO(g)+H2(g) △H=+131kJ/mol
C(s)+O2(g)=CO2(g) △H=-394kJ/mol
CO(g)+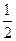 O2(g)=CO2(g) △H=-283kJ/mol
O2(g)=CO2(g) △H=-283kJ/mol
CO(g)+H2O(g)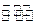 H2(g)+CO2(g)
H2(g)+CO2(g)
下图能表示CO与H2O(g)生成CO2和H2的反应过程和能量关系的图是 (填序号)。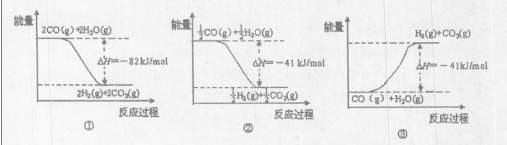
(5)已知830℃时,CO(g)+H2O(g)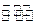 H2(g)+CO2(g)的平衡常数K=1,等物质的量的CO和H2O反应达到平衡时,CO的转化率为 .
H2(g)+CO2(g)的平衡常数K=1,等物质的量的CO和H2O反应达到平衡时,CO的转化率为 .
(6)煤气化过程中会生成少量CH4,已知CH4与CaSO4反应生成CaS、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为 。
(7)煤气化后,混合气体由CO、H2和CH4等组成,可用于制燃料电池。其中碱性条件下CH4参与反应的电极反应式为 。
最近几年我国已加大对氮氧化物排放的控制力度。消除氮氧化物污染有多种方法。
(l)用CH4还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
②CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
③H2O(g)= H2O(l)△H=-44.0kJ·mol-1
CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式为。
(2)用活性炭还原法也可处理氮氧化物。有关反应为:2C(s)+2NO2(g)=N2(g)+2CO2(g) △H<0,起始时向密闭容器中充入一定量的C(s)和NO2(g),在不同条件下,测得各物质的浓度变化状况如下图所示。
①0〜10min内,以CO2表示的平均反应速率v(CO2)=。
②0~10min,10〜20 min,30〜40 min三个阶段NO2的转化率分别为α1、α2、α3,其中最小的为,其值是。
③计算反应达到第一次平衡时的平衡常数K=。
④第10min时,若只改变了影响反应的一个条件,则改变的条件为(填选项字母)。
A.增加C(s)的量 B.减小容器体积 C.加入催化剂
⑤20~30min、40〜50 min时体系的温度分别为T1和T2,则T1_____T2(填“> “<”或“=”), 判断的理由是。
芳香化合物A、B互为同分异构体,B的结构简式是CH3COO- -COOCH2CH3,A经①、②两步反应得C、D和E,B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如下图所示:
-COOCH2CH3,A经①、②两步反应得C、D和E,B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如下图所示: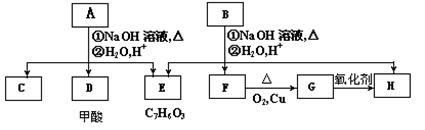
(1)B可以发生的反应类型有(填序号)。
①加成反应 ②酯化反应 ③消去反应 ④取代反应 ⑤聚合反应
B的核磁共振氢谱中会出现_______个峰。
(2)E中含有官能团的名称是。
(3)A有两种可能的结构,其对应的结构简式为,。
(4)B、C、D、F、G化合物中互为同系物的是。
(5)F与H在浓硫酸作用下加热时发生反应的方程式为:
。
硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)硅在元素周期表中的位置是_______。
(2)工业生产粗硅的反应有:SiO2+2C Si(粗)+2CO↑,SiO2+3C
Si(粗)+2CO↑,SiO2+3C SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为。
SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为。
(3)工业上可以通过如下图所示的流程制取纯硅:
①若反应I为 Si(粗)+3HCl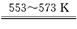 SiHCl3+H2,
SiHCl3+H2,
则反应II的化学方程式为。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另 一种物质,写出该反应的化学方程式:。
③假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%,则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是。
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
CO(g)+2H2(g) CH3OH(g) ΔH
CH3OH(g) ΔH

(1)根据图1请写出合成甲醇的热化学方程式
(热量用E1、E2或E3表示)。
(2)该反应的逆反应速率随时间变化的关系如上图2。t1时改变了某种条件,改变的条件可能是。
(3)判断反应达到平衡状态的依据是(填字母序号,下同)。
| A.2v(H2)(逆) =v(CO)(正) |
| B.混合气体的密度不变 |
| C.混合气体的平均相对分子质量不变 |
| D.CH3OH、CO、H2的浓度都不再发生变化 |
E.容器内CO、H2、CH3OH的浓度之比为1:2:1
(4)在一定温度下,若将4a mol H2和2amol CO放入2L的密闭容器中,充分反应后测得CO的转化率为50%,则该反应的平衡常数为。若此时再向该容器中投入a mol CO、2amol H2和amol CH3OH,判断平衡移动的方向是(“正向移动”“逆向移动”或“不移动”);与原平衡相比,CO的物质的量浓度(填“增大”、“不变”或“减小”)。
(5)某甲烷燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见右图)。A物质的化学式是_________;该原电池的负极反应式可表示为。
塑化剂又称增塑剂,是一种增加材料的柔软性或使材料液化的添加剂。增塑剂 DEHP(C24H38O4)可通过下列流程制备,其中A的主链上有6个碳原子,D是对二甲苯的一种同分异构体,E的苯环上存在2种不同化学环境的氢原子。
回答下列问题:
(1)E的结构简式是_____
(2)B→C的反应类型是_____。
(3)3—甲基庚烷的某同分异构体核磁共振氢谱显示只有一种氢,写出该同分异构体的结构简式并命名:①结构简式__________②命名__________.
(4)DEHP的结构简式是__________
(5)F是E的一种同分异构体,具有如下特征:
a.是苯的邻位二取代物;b.遇FeCl3溶液呈紫色;c.能与碳酸氢钠溶液反应。
写出F与NaHCO3溶液反应的化学方程式:____________________;