对于反应:2SO2+O2  2SO3,当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入空格里(填写“增大”“减小”“不变”)
2SO3,当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入空格里(填写“增大”“减小”“不变”)
| 编号 |
改变的条件 |
化学反应速率 |
| ① |
降低温度 |
|
| ② |
增大O2的浓度 |
|
| ③ |
使用V2O5作催化 剂 剂 |
|
| ④ |
压缩体积 |
|
已知: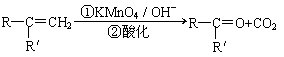
(R、R'可表示烃基或官能团)
A可发生如下转化(方框内物质均为有机物,部分无机产物已略去):
请回答:
(1)F的蒸气密度是相同条件下H2密度的31倍,且分子中无甲基。已知1 mol F与足量金属钠作用产生H2 22.4 L(标准状况),则F的分子式是,名称是。
(2)G与F的相对分子质量之差为4,则G具有的性质是(填字母)。
a.可与银氨溶液反应 b.可与乙酸发生酯化反应
c.可与氢气发生加成反应 d.1 mol G最多可与2 mol新制Cu(OH)2发生反应
(3)D能与NaHCO3溶液发生反应,且两分子D可以反应得到含有六元环的酯类化合物,E可使溴的四氯化碳溶液褪色,则D→E的化学方程式是,
该反应类型是反应。
(4)H与B互为同分异构体,且所含官能团与B相同,则H的结构简式可能是:
、。
(5)A转化为B和F的化学方程式是。
在中学化学中,常用作氧化剂的物质有、、(列举出三种),常用作还原剂的物质有、、(列举出三种)。
(共13分)已知有以下物质相互转化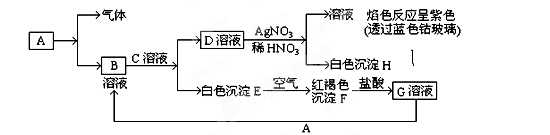
试回答:(1)写出B的化学式,D的化学式。
(2)写出由E转变成F的化学方程式。
(3)写出用KSCN鉴别G溶液的离子方程式;
向G溶液加入A的有关离子反应方程式。
某溶液中含有Al3+,Cu2+,Ag+,现用NaOH溶液、盐酸和试剂X将这三种离子逐一沉淀分离。其流程图如图: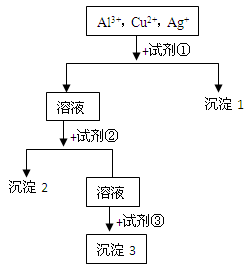
(1)试剂X要过量,其化学式为,是图中的试剂(选填①、②或③)。
(2)沉淀的化学式:沉淀1,沉淀2,沉淀3。
(3)写出混合液+试剂①的离子方程式;
溶液+试剂②的离子方程式
,。
请你按要求填写下表,以除去下列物质中所混有的少量杂质。
| 混合物 |
实验方案 |
反应化学方程式 |
(1)铁粉中 混有少量铝粉 混有少量铝粉 |
||
| (2)Na2CO3固体中混有少量NaHCO3 |
||
(3)FeCl3溶液 中混有少量FeCl2 中混有少量FeCl2 |