汽油不仅是重要的燃料,而且是重要的化工原料,可以通过汽油裂解得到化工原料如乙烯等,还可以在催化剂作用下改变汽油分子的结构,由链烃变为芳香烃,这种变化叫做异构化。下面是以石油为原料发生的有机物的衍变关系图: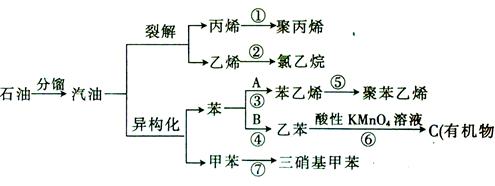
(已知:反应③,④中的原子利用率均为100%)
请回答下列问题:
(1)上述反应①~⑦中属于加成反应的有___________________(填序号,下
同),属于取代反应的有__________________。
(2)写出A,B的结构简式:A______________,B________________。
C的分子式为_________________。
(3)写出下列反应的化学方程式:
④________________________________________________________________;
⑦____________________ ____________________________________________。
____________________________________________。
有一固体混合物可能含有氯化铁、亚硝酸钠、硝酸银、氯化铜、硝酸钠、熟石灰和氯化铵等7种物质。将混合物溶于水得白色沉淀和无色溶液。白色沉淀可溶于氨水中。无色溶液与强碱共热放出的气体可使酚酞变红。无色溶液也可使酸性高锰酸钾溶液褪色。无色溶液受热时可放出氮气。
已知:Ksp(AgNO2)=6.0×10-4;Ksp(AgCl)=1.56×10-10
回答下列问题(用化学符号回答):
(1)该固体混合物中肯定存在的物质是________________,肯定不存在的物质是_______________。
(2)混合物溶于水时所得的白色沉淀中肯定有________________。该沉淀溶于氨水的离子方程式为_______________________________________。
(3)无色溶液中,使酸性高锰酸钾褪色的物质是___________________。
(4)写出无色溶液受热时放出氮气的化学方程式__________________。
向含0.2molAl3+的明矾溶液中逐渐加入2mol/LBa(OH)2溶液时,测得产生沉淀质量m(g)和逐渐加的2mol/LBa(OH)2溶液的体积(mL)的关系如下图,试填写空白
(1)写出OA段反应的离子方程式
OA;
(2)m1 = V1 =
m2 =V2=
图中字母所代表的物质均为中学化学常见物质。其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料;常温下C、D、H为气体单质。单质E、M、N为金属,N是地壳中含量最大的金属元素。Y是红褐色沉淀。这些物质在一定条件下存在如下转化关系,其中有些反应物或生成物已经略去。试回答下列问题:
(1)Z→L反应的名称是。
(2)K的电子式为。
(3)写出B→F的离子方程式。
(4)写出K与CO2反应的化学方程式。
(5)Y与NaClO和B的混合溶液作用,是制备绿色水处理剂(Na2MO4)的一种方法,请写出该反应的离子方程式。
已知硝酸与金属发生氧化还原反应的时候,一般硝酸浓度越稀,对应的还原产物中氮的化合价越低。现有一定量的铝、铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4 mol/L NaOH溶液,所加NaOH溶液的体积(V)与产生沉淀的物质的量(n)关系如图所示。则:
(1)试写出DE段、EF段所发生反应的离子方 程式:
程式:
DE段
EF段
(2)合金中铝的物质的量为mol
(3)合金中金属的物质的量共为mol
(4)求出C点的值为ml
汽车安全气囊 是行车安全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气囊工作的化学原理,取安全装置中的固体粉末进行实验。经组成分析,确定该粉末仅Na、Fe、N、O四种元素。水溶性试验表明,固体粉末部分溶解。经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸。取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72L。
是行车安全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气囊工作的化学原理,取安全装置中的固体粉末进行实验。经组成分析,确定该粉末仅Na、Fe、N、O四种元素。水溶性试验表明,固体粉末部分溶解。经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸。取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72L。 单质乙就在高温隔绝空气的条件下与不溶物红棕色粉末反应生成化合物丙和另一种单质。化合物丙与空气接触可转化为可溶性盐。
单质乙就在高温隔绝空气的条件下与不溶物红棕色粉末反应生成化合物丙和另一种单质。化合物丙与空气接触可转化为可溶性盐。
请回答下列问题:
(1)甲的化学式为,丙的电子式为。
(2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为。
(3)单质乙与红棕色粉末发生反应的化学方程式为,安全气囊中红棕色粉末的作用是。
(4)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是。
| A.KCl | B. KNO3 KNO3 |
C.Na2S | D.CuO |